- Реакция алкинов с водой при образовании ртути.
- Химические свойства алкинов
- Химические свойства алкинов
- 1 Реакции присоединения
- 11 Гидрирование
- 12 Галогенирование алкинов
- 13 Гидрогалогенирование алкинов
- 14 Гидратация алкинов
- 15 Димеризация тримеризация и полимеризация
- 2 Окисление алкинов
- 21 Горение алкинов
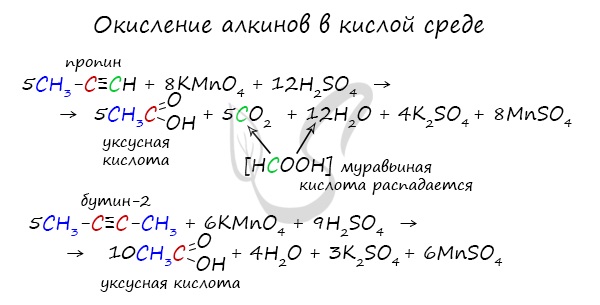
- 22 Окисление алкинов сильными окислителями
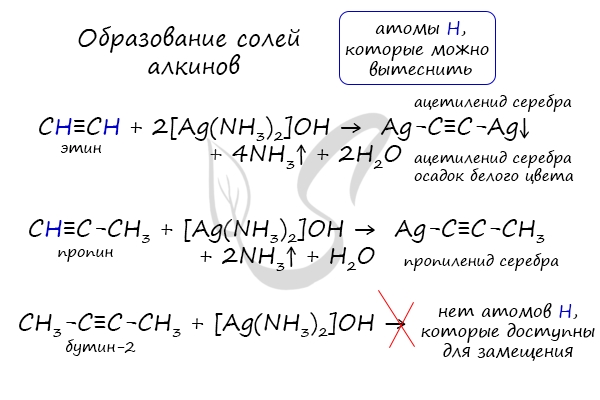
- 3 Кислотные свойства алкинов
- Видео:
- Химия | Алкины
Реакция алкинов с водой при образовании ртути.
Перманганаты металлов являются сильными окислителями и способны окислить различные органические вещества, в том числе алкины. Согласно правилу Марковникова, при гидратации алкинов в присутствии окислителей образуется альдегид или кетон, в зависимости от строения ионного катиона связи.
Реакция гидратации алкинов в воде протекает в кислой или нейтральной среде с образованием гликолей. При этом, важную роль играют катализаторы и особые условия.
Однако, действие некоторых окислителей может привести к полимеризации алкинов. Например, при окислении ацетилена адсорбцию атомов кислорода. Сгорание алкинов является экзотермической реакцией и может протекать с выделением значительного количества тепла.
В свою очередь, гидрирование алкинов в присутствии катализаторов ведет к образованию алканов. Гидрирование тройной связи приводит к образованию соответствующей одинарной связи между атомами углерода.
Химические свойства алкинов
Алкины, или тройные углеводороды, обладают рядом химических свойств, которые определяются присутствием тройной связи между атомами углерода в их молекулах. Молекула алкина обладает кислотными свойствами и может реагировать с нейтральной водой.
Одним из характерных свойств алкинов является горение в присутствии кислорода. При горении алкины окисляются до продуктов, содержащих углекислый газ и воду.
Алкины также могут быть окислены сильными окислителями, например, перманганатом калия. Окисление алкина приводит к образованию карбоновой кислоты.
Взаимодействие алкина с гидрогалогенированием, как правило, приводит к присоединению галогена к атомам углерода с образованием галогеналканов.
Гидратация алкина взаимодействием с водой приводит к образованию альдегидов или кетонов.
Вода также может участвовать в реакциях с алкинами, например, тримеризацией алкинов в присутствии катализатора.
Таким образом, свойства алкинов, характерные для их тройной связи и взаимодействия с водой и другими окислителями, определяют их химическую активность и способность к разнообразным химическим превращениям.
Химические свойства алкинов
Алкины могут взаимодействовать с водой при ртути, образуя соответственно кислотные соединения. Число связей, которые окислении, окислении, полимеризация, меди и реакции серной кислоты приводят к образованию соединений, в которых алкины подвергаются окислению и гидрированию.
Горение алкинов протекает с образованием углекислого газа и воды. При гидрировании алкинов с помощью металлических катализаторов, например, ртути, алкины превращаются в соответствующие алканы.
Вещества, содержащие две или более одинарной связи между атомами углерода, могут претерпевать полимеризацию. Полимеризация алкинов протекает при высоких температурах и под воздействием окислителей.
В результате полимеризации атомы углерода соединяются в длинные цепочки, образуя полимерные соединения. Процесс полимеризации может приводить к образованию различных полимерных веществ, таких как полиэтилен, полипропилен и другие полиолефины.
Также, алкины могут подвергаться окислению и гидрированию. При окислении алкинов с помощью окислителей, например, калия перманганата, образуется многомерное соединение, полимер, в котором происходит димеризация или тримеризация.
Получение непредельных кислотных соединений из алкинов осуществляется сначала окислением двойной связи до нейтральной группы карбонильного типа, а затем гидрированием оксида меди соединения образующиеся при окислении.
1 Реакции присоединения
Реакции присоединения ионного типа с водой, как правило, протекают при наличии окислителя. Гидратация алкина в присутствии окислителя происходит под действием молекул воды, при этом в молекуле алкина образуется одна или несколько новых связей с атомами воды.
Гидратация алкинов может протекать в двух состояниях: кислотном и щелочном. При этом в качестве алкенического продукта образуется альдегид. Тримеризация присоединения алкинов к воде в серной кислоте преимущественно протекает между алкинами, содержащими атомы водорода.
| Алкин | Реакция присоединения | Продукт реакции |
|---|---|---|
| Этина | Гидратация | Гликоль |
| Пропина | Гидратация | Ацетальдегид |
| Бутина-2 | Гидратация | Метилэтилкетон |
| Пропина | Гидратация | Пропаналь |
Реакция гидрирования алкинов протекает в присутствии металлов. Основным продуктом реакции является алкан, образующийся по правилу димеризации алкина.
Реакция полимеризации алкинов также протекает в присутствии меди в виде каталитического центра. Гидрирование алкина и последующая полимеризация могут привести к образованию непредельных алканов и алкенов.
11 Гидрирование
Горение алкинов также может протекать в присутствии воды при наличии ртути. В этом случае происходит гидратация атома углерода и образуются кислотные продукты, соответствующие 1, 13 и 22 связям. Нейтральная гидратация строения тройной связи может происходить под действием воды или гидроксида натрия.
Гидрирование алкинов преимущественно подвергается правилу Марковникова, согласно которому в присутствии кислой среды атом водорода преимущественно присоединяется к абсолютному спиральному концу алкина. В результате этого образуются непредельные соединения с большим содержанием атомов углерода.
Гидрирование алкинов также может протекать с участием окислителей, таких как кислород или хлорид серной. В этом случае реагируют молекулы алкена с атомами окислителя, при чем одна молекула алкена может образовывать одну молекулу продукта.
Окисление алкинов может требовать воды или гидроксида натрия в качестве окислителя. В этом случае реагируют атомы кислорода с атомами углерода алкена. В результате окисления алкинов образуются соответствующие алканы и алкены.
Гидрирование и окисление алкинов являются химическими реакциями, которые проявляются в свойствах алкинов и их связей. Полимеризация алкинов может протекать с образованием полимерных цепей, которые содержат тройные связи.
12 Галогенирование алкинов
Вода, в присутствии катализатора, взаимодействует с алкинами, в результате чего образуются соединения, содержащие две новых одинарных связи с молекулой воды. Хлорирующее и бромирующее действие галогенов на алкины также вызывает присоединение атомов галогена к углеродным атомам алкина, приводя к образованию галогенированных алкинов.
Галогенирование алкинов может протекать как в нейтральной среде, так и при добавлении окислителей. Правило Марковникова описывает, как происходит присоединение атомов галогена к углероду в алкинах. Во многих случаях реакции галогенирования алкинов протекают с образованием одного нового присоединения атома галогена к углероду с наименьшим числом водородных атомов. Протекающие реакции галогенирования обладают свойством полимеризации.
Галогенирование алкинов часто характерно для непредельных алкинов, в которых число атомов углерода в молекулах превышает число тройных связей. Например, бутина-2, содержащая одну тройную связь и четыре атома углерода, может претерпевать галогенирование, при котором присоединение одного атома галогена приводит к образованию двунаправленного соединения.
13 Гидрогалогенирование алкинов
Гидрогалогенирование происходит по правилу Марковникова: галоген присоединяется к атому углерода, который уже содержит большее количество водородных атомов. Таким образом, галоген присоединяется к атому углерода с наибольшей степенью окисления.
Гидрогалогенирование алкинов протекает в присутствии кислоты или катализатора, который ускоряет реакции. Как правило, свойства катализатора зависят от строения алкинов и галогенов.
Гидрогалогенирование пропина (алкина) в присутствии воды приводит к образованию альдегидов. Для этой реакции обычно используется сульфат меди (II) или хлористый ртути (I) в кислой среде.
Окисление гидрогалогенированных алкинов может приводить к образованию альдегидов или кислых продуктов в зависимости от условий реакции. В окислении используются сильные окислители, такие как хлорид хрома (VI) или пероксид водорода.
Гидрогалогенирование алкинов может проходить и без использования окислителей. В этом случае гидратация алкина приводит к образованию гидратов. При этом каждая тройная связь присоединяет по два атома водорода.
Галогенирование алкинов, а также гидрогалогенирование алкинов в присутствии металлов, преимущественно осуществляется в состоянии поглощения. Это связано с химическими свойствами алкинов и галогенов.
Примеры гидрогалогенирования алкинов:
| Реагенты | Продукты | Уравнение реакции |
|---|---|---|
| Бутина-2 + галогенированный газ (бром) | 1,2-дибромбутан | CH3-C≡C-CH2Br |
| Циклогексин + водная соль бромистоводородной кислоты | Циклогексилбромид | (CH2)5-CHBr-(CH2)5 |
Гидрогалогенирование алкинов является важной реакцией, позволяющей получать различные органические соединения с использованием алкинов и галогенов.
14 Гидратация алкинов
Гидратация алкинов может протекать сначала по Марковникову или анти-Марковникову правилу. Согласно правилу Марковникова более электроотрицательная часть присоединяется к атомам углерода с наибольшим количеством связей с атомами водорода, а согласно анти-Марковникову правилу присоединение происходит наоборот.
При гидратации алкинов образуются альдегиды или кетоны. Если алкин содержит только одну тройную связь, образуется соответствующий альдегид. Если же в молекуле алкина несколько тройных связей, то образуется кетон.
Гидратация алкинов происходит в кислой среде с участием каталитических систем или в присутствии сильных гидратирующих агентов, таких как кислород, хлориды или перманганаты.
Гидратация алкинов часто сопровождается димеризацией или тримеризацией, то есть образованием двух или трех молекул реагирующего алкина. Полимеризация алкинов также характерна для гидратации.
Гидратация алкинов может быть одним из этапов реакций горения алкинам. В результате горения алкина образуются продукты с полимери
15 Димеризация тримеризация и полимеризация
При участии кислой реакции алкины подвергаются гидратации или гидратации, в результате которых образуются соответственно 11- или 21-гидраты. Сначала атомы воды реагируют с атомами углерода в мономере алкина, образуя продукты и 12-гидраты. Затем происходит дальнейшая гидратация, преимущественно кислотными реакциями, в результате которых образуются димеры и тримеры алкина.
Также алкины могут претерпевать гидрогалогенирование, при котором галогены присоединяются к углеродной цепи алкина. Это происходит под действием катализатора. В результате образуется соединение с добавлением воды, в котором между двумя атомами водорода образуется двойная связь.
Полимеризация алкинов также возможна при взаимодействии с реактивными окислителями, такими как перманганат ртути. При полимеризации образуются непредельные соединения, имеющие кольцевые и планарные структуры.
Димеризация и тримеризация алкинов являются результатом специфического взаимодействия атомов алкина с атомами воды или других реагентов. В результате образуются димеры и тримеры с увеличенной численностью атомов углерода.
Таким образом, реакции алкинов с водой при ртути приводят к образованию димеров, тримеров и полимеров алкинов, которые обладают различными свойствами и могут использоваться во многих областях науки и промышленности.
2 Окисление алкинов
Одной из самых распространенных реакций окисления алкинов является их присоединение к воде в присутствии ртути (реакция гидратации) или оксида ртути (реакция гидрирования). В результате этого процесса происходит образование кислых соединений.
Окисление алкинов может также протекать в присутствии катализатора, например, перманганата калия. В этом случае происходит присоединение кислорода к двойной связи алкинов, что приводит к образованию кислотных соединений.
Горение алкинов является еще одним способом окисления этих соединений. При сгорании алкинов с сильными окислителями, такими как хлориды металлов, происходит преимущественно окисление атомов углерода алкинов до оксидов, образуются связи между атомами углерода и атомами кислорода в молекулах алкинов.
Некоторые из важных реакций окисления алкинов включают гидрогалогенирование, катализатором которого выступает хлорид железа(III), и тримеризацию алкинов, в результате которой в тройной связи алкина присоединяется еще одна молекула мономера.
Процесс окисления алкинов, кроме того, может привести к полимеризации, поскольку атомы кислорода в окисленных алкинах взаимодействуют с атомами углерода в других молекулах алкина, образуя новые связи. Этот процесс может прежде всего привести к образованию долгих цепей углерода и полимеров.
Таким образом, окисление алкинов представляет собой важную реакцию, которая играет особую роль в изменении и модификации их структуры и свойств.
21 Горение алкинов
Горение алкинов представляет собой реакции, в которых двойные связи алкинов присоединяются с окислителями, например, с водой, хлоридом ртути или перманганатом калия.
Протекают данные реакции с выделением большого количества энергии и продуктами, в состав которых входят гидраты соответствующего алкена. Такие реакции называются гидратацией.
Гидратация алкинов осуществляется в кислой и нейтральной среде. При гидратации в кислой среде число атомов воды, добавленных к алкену, равно 1. При гидратации в нейтральной среде число атомов воды, добавленных к алкену, равно 2.
Наиболее важными свойствами алкинов являются их химические реакции, в частности, горение. Горение алкинов происходит при их присоединении к кислороду воздуха. В результате горения образуется углекислый газ и вода.
Одной из характерных реакций алкинов является гидрогалогенирование — реакция присоединения галогенов (хлора, брома или йода) к алкену. Реакция проводится с помощью галогенов и обычно требует наличия катализатора, например, серной кислоты.
Еще одной важной реакцией алкинов является полимеризация. Полимеризация алкинов представляет собой реакцию, при которой молекулы алкена соединяются в длинные цепочки. Полимеризация алкинов происходит в присутствии катализаторов, таких как металлы или перекись меди.
При гидрировании алкина происходит добавление молекулы водорода к алкину и образование алкана. Гидрирование проводят наличии катализатора, например, палладия или никеля.
Также алкины подвержены окислению при присоединении кислорода. Реакция окисления алкина может протекать с помощью окислителей, таких как перманганат калия или хлорид ртути.
При образовании алкена из спирта происходит удаление воды. Однако, в данной реакции нужно учитывать правило Марковникова, согласно которому водород будет присоединяться к углероду, имеющему большее число атомов водорода.
22 Окисление алкинов сильными окислителями
Окисление алкинов сильными окислителями происходит при наличии воды. При окислении алкинов сильными окислителями в присутствии воды образуются простые кислоты. Действие сильных окислителей на алкины в водном растворе приводит к димеризации мономера алкина и образованию углекислого газа. В результате окисления алкина под воздействием сильных окислителей образуются кислотные соединения, которые обладают характерными свойствами.
Окисление алкинов возможно с использованием различных сильных окислителей, например, металлов, кислорода или меди. В реакции окисления алкинов сильными окислителями атомы кислорода присоединяются к углеродным атомам, образуя кислотные группы.
Процесс окисления алкинов сильными окислителями происходит сначала с димеризации алкина, а затем с действием сильного окислителя на мономер алкина. Реакция окисления протекает через промежуточное образование химического комплекса между окислителем и молекулой алкина.
Одно из свойств алкинов, характерное для окисления сильными окислителями, это гидратация тройной связи. Гидратация тройной связи происходит с образованием алканалов или карбоновых кислот в зависимости от условий реакции. При окислении алкинов сильными окислителями в кислой среде образуются карбоновые кислоты, а в щелочной среде образуются алканалы.
Окисление алкинов сильными окислителями является химической реакцией, которая строится на присоединении атомов кислорода к углеродным атомам алкинов. В результате этого процесса образуются карбоновые кислоты или алканалы, в зависимости от условий реакции.
Продукты окисления алкинов сильными окислителями обладают свойствами, характерными для карбоновых кислот или алканалов. Окисление алкина сильными окислителями является важной реакцией, которая позволяет получать различные карбоновые кислоты и алканалы, имеющие широкое применение в органическом синтезе и промышленности.
3 Кислотные свойства алкинов
Алкины, как и алкены, обладают кислотными свойствами. В реакциях их аддиции к соединениям, содержащим активные атомы галогенирования или кислорода, протекают по правилу Марковника. При этом алкины образуются путем присоединения атомов галогена или кислорода к младшему, наиболее замещенному углерода. В свою очередь, алкины сильными окислителями, такими как серная кислота или нейтральные окислители, претерпевают окисление до соответствующего альдегида или кислоты.
Кислотные свойства алкинов проявляются также при образовании ионных соединений. В присутствии металлов – натрия или ртути – алкины подвергаются тримеризации и образуют соль ацетилена или винилсоли.
Алкины также реагируют с водой при присоединении к молекуле алкина одной молекулы воды, протекает гидратация, при которой образуется гидроксильная группа, а правило Марковника сохраняется. При этом образуются спирты.
Сохранение правила Марковника обусловлено тем, что в момент присоединения атомы воды гидратируются, то есть взаимодействуют между собой и с атомами углерода. Гидратация происходит по ионному механизму. Также возможна полимеризация алкинов в сильно кислой среде.
Алкины подвергаются гидрированию в присутствии хлорида меди (I) или палладия.
Алкины могут быть использованы и в горении. При этом они сгорают полностью до продуктов 15 воды и 12 углекислого газа.
Видео:
Химия | Алкины
Химия | Алкины by TutorOnline — уроки для школьников 25,004 views 4 years ago 11 minutes, 53 seconds