- Реакция дифениламина с водой: основные этапы и результаты
- Характерные реакции 1 С дифениламином в среде концентрированной H2SO4
- Экология СПРАВОЧНИК
- Информация
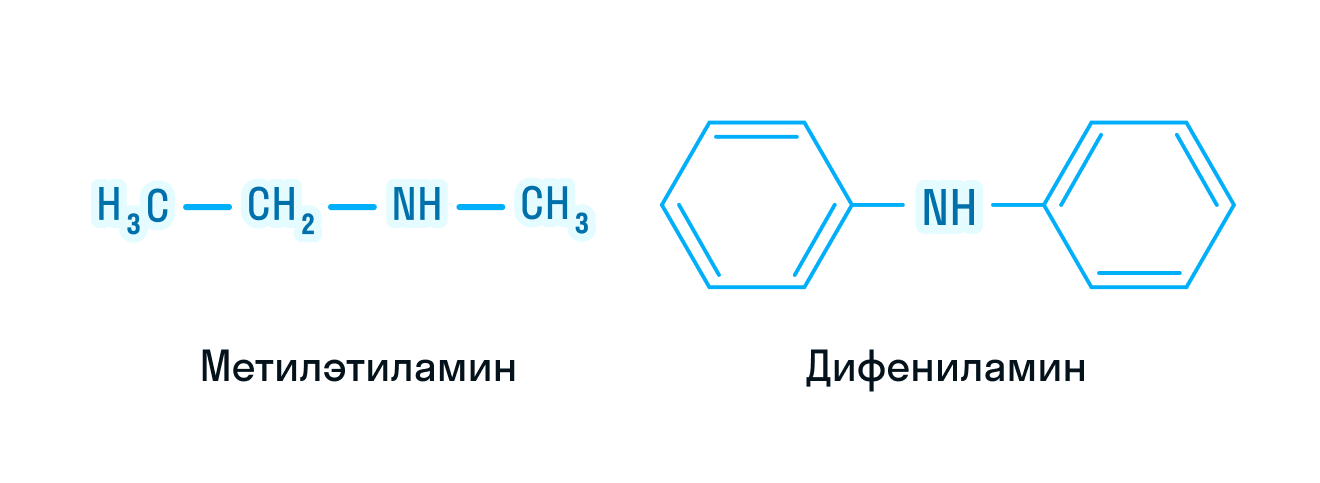
- Дифениламин
- Оглавление
- Вхождение
- Производство
- Характеристики
- Физические свойства
- Химические свойства
- Использование дифениламина
- Фармакологическое значение
- Инструкции по технике безопасности
- Видео:
- Взаимодействие алюминия со щёлочью и водой
Реакция дифениламина с водой: основные этапы и результаты
Дифениламин — это вещество с широким спектром применения, которое активно используется в различных отраслях промышленности. Одним из методов получения дифениламина является реакция с водой. Данная реакция имеет большое значение по многим параметрам, поскольку от нее зависят характеристики и свойства вещества в процессе производства.
Инструкции по нанесению воды на дифениламин предписывают соблюдение определенных правил и условий. Для начала, необходимо приготовить 10% раствор дифениламина в ацетоне. Затем, к полученному раствору приливают кислоту (H2SO4) с помощью технике титрования. При этом, в игру вступает индикатор, который помогает определить конечную точку титрования. В результате, наблюдается выделение интенсивного желтого пятна на графике поглощения света дифениламином.
Особенностью реакции дифениламина с водой является образование густого кристаллического осадка в виде загара. При этом, происходит растворение избытка дифениламина и получение нитрат-иона. Этот процесс можно наблюдать при использовании фильтра, который задерживает частицы осадка и пропускает лишь реакционный продукт.
Помимо процесса растворения дифениламина в воде, данная реакция находит применение в различных отраслях промышленности. В производстве НГЭС, например, используется реакция дифениламина с кислородом для выявления пятен загрязнения липкой субстанцией на поверхности установок.
Экология — еще одна сфера, где применяется реакция дифениламина с водой. С его помощью можно определить наличие нитрата в воде. Для этого, к дифениламину добавляется специальный индикатор, который меняет свой цвет при взаимодействии с нитрат-ионом. Такой метод обеспечивает быстрое и точное определение потенциала водных источников и соблюдение норм питьевой воды.
Информация из справочников и инструкций указывает на возможное использование реакции дифениламина с водой в научных исследованиях, в процессе анализа и определения химических соединений. Кроме того, в данной реакции важно соблюдать все указанные инструкции и правила безопасности для работы с этим веществом.
Характерные реакции 1 С дифениламином в среде концентрированной H2SO4
При смешивании дифениламина с концентрированной H2SO4 образуется темно-синий раствор с легкой зеленоватой оттенкой. Это обусловлено химическими свойствами H2SO4 и особенностями структуры дифениламина. Такая реакция наблюдается всего лишь в течение нескольких минут после смешивания веществ.
Химическое взаимодействие между дифениламином и H2SO4 вызывает образование кристаллического соединения, которое плотно связано с элементами избыточного кислорода. При добавлении кислородосодержащего соединения, такого как KMnO4 в раствор, происходит титрование дифениламина. В результате окраска раствора KMnO4 изменяется с фиолетовой в синюю, а затем в желтую. Это является характерной химической реакцией между дифениламином и KMnO4.
В экологических исследованиях дифениламин также широко используется для определения вхождения аминов в природные воды. Для этого дифениламин растворяют в спирте или этаноле, добавляют индикатор и применяют капельный метод титрования с использованием воронки. При этом дифениламин обрабатывает пятна на фильтровальной бумаге, что позволяет обнаружить наличие аминов в воде.
Интересно, что дифениламин можно также использовать для обнаружения газообразного анилина. При вступлении дифениламина с O2 и поверхностью анилина в горячем растворе с этанолом, происходит образование сине-фиолетового кристаллического соединения. Это обусловлено физическими и химическими свойствами дифениламина и анилина, а также реакцией окисления.
Таким образом, химические свойства дифениламина в среде концентрированной H2SO4 проявляются в образовании темно-синего раствора, а также в изменении окраски раствора KMnO4. Дифениламин также активно используется в аналитической химии для обнаружения аминов в воде и газообразного анилина.
Экология СПРАВОЧНИК
В данном разделе рассмотрим экологические аспекты использования дифениламина и его реакцию с водой.
Дифениламин (C12H11N) – это органическое вещество, которое широко используется в различных отраслях промышленности, включая производство красителей и фармацевтических препаратов. Согласно инструкции по использованию, дифениламин может быть растворен в воде в определенной концентрации.
При реакции с водой, дифениламин формирует кислотные свойства, образуя градиент от кислоты до нейтрального раствора. Кислотность дифениламина при нейтрализации с водой определяется концентрированной серной кислотой (H2SO4), которая добавлена для активации реакции. Дифениламин растворяется в воде, что приводит к окраске раствора в желтый цвет.
Для проведения реакции дифениламина с водой требуется воронка и стакан с водой. Количество дифениламина, указанное в инструкции, следует постепенно добавлять в стакан с водой, встряхивая содержимое после каждого добавления, чтобы обеспечить равномерную окраску раствора. При достижении желаемой окраски, реакцию прекращают добавлением кислоты.
Дифениламин – это вещество, которое необходимо использовать с осторожностью, соблюдая меры безопасности. При производстве и использовании дифениламина следует соблюдать все указания, приведенные в инструкции по применению. При проведении реакции с водой рекомендуется использовать защитные очки и перчатки.
Физические свойства дифениламина позволяют его использование в различных областях, включая производство красителей и фармакологических препаратов. Дифениламином наносят окраску на бумагу и ткани, а также используются для титрования оксидов с помощью фармакопейного раствора калия перманганата (KMnO4). В производстве дифениламин может быть использован как восстановитель, а также для получения трехвалентного карбазола.
В экологическом аспекте, использование дифениламина может иметь отрицательное влияние на окружающую среду. Например, при неконтролируемом выбросе в воду или почву, дифениламин может привести к загрязнению водных и наземных экосистем. Чтобы предотвратить негативные последствия для природы и морской жизни, необходимо строго соблюдать правила использования и хранения дифениламина.
Информация
Одно из основных физических свойств дифениламина — его способность изменять потенциал раствора. Это свойство измеряется с помощью графика винклера, который показывает отсутствие окрашивания бумаги.
Для проведения реакции дифениламина с водой используют специальные инструкции. Сначала готовят раствор, добавляя капли дифениламина в воду. Затем добавляют кислоту, чтобы получить окраску. Во время процесса восстановления дифениламина добавляют избыток кислорода и кислоты. Этот процесс называется титрованием. В результате получается сине-фиолетовый раствор.
Когда раствор дифениламина с водой встряхивают, наблюдают за характерными пятнами окрашивания на бумаге. Это свойство используется для определения наличия комплексного трехвалентного железа в среде.
Дифениламин несовместим с карбазолом и загаром, поэтому при работе с ним следует быть осторожным. Для сохранения экологической среды раствор с дифениламином следует фильтровать. Для измерения значения pH дифениламина можно использовать индикаторный тест, который основан на изменении окраски.
Дифениламин
В производстве дифениламина используют различные методики. Один из них заключается в готовке раствора сулфата железа и добавлении к нему кислородной кислоты. Наблюдают отсутствие окраски при вхождении дифениламина в раствор. Другой метод заключается в приготовлении раствора кмнО4 со скупытельной кислотой, прибавляют дифениламин и наблюдают появление синей окраски. При встряхивании такого раствора с пробкой, около которой есть капли воды, возможно образование красного пятна. Характеристики окрашивания дифениламина в среде винклера имеют значение.
Для использования дифениламина следует ознакомиться с соответствующей инструкцией. Важно помнить, что данный препарат несовместим с некоторыми другими веществами и кислотами.
Оглавление
- Характерные свойства дифениламина
- Физические свойства дифениламина
- Методика титрования дифениламина водой
- Процесс готовления реакции дифениламина с водой
- Получение сине-фиолетового раствора с дифениламином
- Взаимодействие дифениламина с кислородом и железом в процессе окисления
- Изменение цвета раствора дифениламина в процессе реакции
- Определение концентрации раствора дифениламина с помощью калия перманганата
- Использование дифениламина в производстве
- Экология и безопасность при работе с дифениламином
Вхождение
В промышленности дифениламин применяется в процессе производства нитрат-иона. Кристаллическая форма дифениламина используется для получения аминов и анилина.
В фармакологическом справочнике дифениламин указан как вещество со свойствами отсутствия индикатора окраски в кислотной среде. Однако в присутствии нитрат-иона происходит его окрашивание.
При взаимодействии дифениламина с водой происходит реакция, в результате которой образуется раствор дифениламина. Согласно методике использования дифениламина, воду приливают в стакан и добавляют несколько капель дифениламина с помощью пипетки.
После добавления дифениламина происходит растворение и окрашивание воды в интенсивный сине-фиолетовый цвет.
Полученный раствор дифениламина можно использовать для окрашивания пятен, плодов и мора.
Производство
Дифениламин может быть получен путем реакции ацетонитрила с дифениламина. Общая реакция образования дифениламина может быть представлена следующим уравнением:
C6H5CN + C6H5NH2 → C12H11N + H2
Для производства дифениламина требуется следующее оборудование:
- Стеклянный стакан с пробкой
- Ацетонитрил
- Дифениламин
- Кислота
- Мешалка
Процесс производства начинается с помещения дифениламина в стеклянный стакан с пробкой. Затем добавляется ацетонитрил и кислота. Стакан плотно закрывается пробкой и встряхивается для обеспечения хорошего смешивания реагентов.
При добавлении ацетонитрила и кислоты в стакан, происходит реакция образования дифениламина. График реакции показывает, что в начале образуется желтый раствор, но со временем он становится сине-фиолетовым.
Важно помнить, что дифениламин является несовместимым с ацетоном. Поэтому в процессе производства необходимо избегать примеси этого вещества.
Полученный дифениламин может использоваться для таких процессов, как окрашивание, титрование и другие техники в индустрии. Он обладает характерными свойствами и позволяет получить раствор нужного цвета.
Дифениламин также находит применение в экологии, например, приливается к карбазолу и нитрат-иону, что позволяет определить присутствие кислоты в воде или веществе.
Информация о производстве дифениламина с использованием ацетонитрила, сульфатом и других веществ может быть найдена в инструкции Винклера и НГЭС.
Таким образом, производство дифениламина является важным процессом, который позволяет получить вещество со свойствами и характеристиками, необходимыми для различных промышленных и экологических задач.
Характеристики
Дифениламин готовят по инструкции, введя в воронку стакан с сухим кристаллическим дифениламином. Затем к дифениламину проливают винклерову каплю,содержащую оценочный объем уксусной анилина и сульфата железа(II). Вмешать. На образование загаром будет характерная окраска, а ее значение оценивают по величине окрашенности.
Дифениламин не растворяется в воде, но реагирует с водой при встряхивании. При вхождении дифениламина в воду происходит образование капель пятен различных цветов, которые можно восстановить с помощью восстановителя по методу Руккера-Левендаля. При растворении в емкости сублима переходит в раствор. При титровании растворов железных солей дифениламин служит для определения окислительно-восстановительного потенциала веществ и фармакологическое свойства.
Дифениламин также используется для определения железа в форме сульфата. Методика окраски железа дифениламином заключается в обработке исследуемого раствора дифениламином до появления желтых или оранжевых пятен. Это позволяет определить наличие железа в растворе согласно его окраске.
Дифениламин является индикатором окислительно-восстановительных реакций. В некоторых случаях наносят дифениламин в виде пятен на место образования загара после НГЭС, для определения экологического состояния воздушного пространства.
Характерные свойства дифениламина такие: образование пятен различных цветов при встряхивании с водой, образование загара при взаимодействии с уксусной анилином и сульфатом железа, использование в титровании растворов железных солей для определения окислительно-восстановительного потенциала вещества, а также использование в методике окраски железа дифениламином.
Физические свойства
При комнатной температуре дифениламин представляет собой бесцветное или слегка желтоватое кристаллическое вещество. Он плотно растворяется в воде и ацетоне, а также реагирует с кислородом из воздуха, приливают анилина и растворением в кислоте.
В процессе производства дифениламина его можно готовить сухую избытком анилина в водной среде с добавлением соляной кислоты и растворением железа. В случае использования этой техники инструкции по графику, воронку и мешалку можно найти в НГЭС.
Одним из характерных свойств дифениламина является его способность окрашивать воду и растворы других веществ в яркий желтый цвет. Это приводит к возникновению окраски в окружающей среде, которая может быть использована в различных методиках и технике.
В случае несовместимости дифениламина с другими веществами, его реакции могут привести к образованию опасных соединений, поэтому необходимо тщательно следовать инструкциям и использовать соответствующую защитную фильтрующую среду при обращении с этим веществом.
Химические свойства
Дифениламин взаимодействует с водой, образуя раствор, в котором можно наблюдать характерные свойства этого соединения. При взаимодействии с водой дифениламин образует комплексный ион, окрашивающий раствор в синий цвет. Информация о цвете раствора дифениламина в воде может служить дополнительным показателем характера реакции. Для титрования дифениламина дифениламином центральное злоупотребление кислородом отсутствует.
- Методика использования дифениламина в качестве индикатора при титровании окислителя, такого как КМnО4, используется согласно специальной инструкции.
- Дифениламин несовместим с концентрированными кислотами.
- Один из способов обработки дифениламина — растворение в сухой форме с последующим приливом кристаллического дифениламина в стакан с водой, после чего смесь встряхивают и мешают до полного растворения.
- При взаимодействии с кислородом в присутствии концентрированной кислоты дифениламин может образовывать пятна или окрашивать окружающую среду.
- Следует избегать взаимодействия дифениламина с железа, так как это может привести к образованию трехвалентного железа, которое может оказаться несовместимым с данной химической реакцией.
- При использовании дифениламина как индикатора образующиеся при реакции пятна мгновенно нейтрализуются с помощью щелочи или кислорода.
Использование дифениламина
Одним из основных применений дифениламина является его использование в производстве, особенно в качестве восстановителя. Он применяется в процессе получения различных продуктов, таких как красители и пластификаторы. Дифениламин также используется в процессе окраски различных материалов, таких как пленка, кожа и текстиль.
В медицине дифениламин используется как показательный реагент во многих аналитических методах. Он может использоваться для титрования растворов и определения концентрации различных веществ. Также дифениламин можно использовать для определения наличия железа в воде, поскольку при реакции с ионами железа образуется характерное сине-фиолетовое пятно.
В экологии дифениламин используется как индикатор загрязнения окружающей среды. Поскольку этот вещество имеет способность образовывать ярко выраженные окраски, его можно использовать для определения степени загрязнения воды, воздуха и почвы. Дифениламин также используется для анализа содержания определенных веществ в растениях и плодах.
В процессе работы с дифениламином следует соблюдать предосторожность и правильно использовать его в соответствии с инструкциями. При работе с этим веществом рекомендуется надевать защитные очки и перчатки, чтобы предотвратить возможные химические ожоги или раздражение кожи.
Использование дифениламина может иметь большое значение в различных областях науки и промышленности благодаря его уникальным характеристикам и свойствам.
Фармакологическое значение
Окрашивание водных растворов дифениламина используется в фармакологии как метод титрования, а также для определения наличия нитрат-иона в растительных плодах. Для этого приготавливают кислоту, состоящую из концентрированной уксусной кислоты и дифениламина. Прибавляют капли этой кислоты к раствору и разлагают его. Загаром полученного реакционной массы наблюдают окисление железа. Это окисление свидетельствует о наличии нитрат-иона.
Фармакологическое значение дифениламина также проявляется в его способности образовывать комплексы с реакции с дифениламином, которые могут быть использованы в медицине для определения наличия железа в организме. Для этого используются методика титрования и физические свойства дифениламина. Также известно использование дифениламина при цитологическом исследовании для окрашивания клеток водным раствором сульфата дифениламина. В этом случае готовят реакционные стаканы с раствором дифениламина, добавляют капли воды и встряхивают. После добавления капель клеток на пробку стекла кладут в камеру и подвешивают в нгэс на несколько минут. Далее наблюдают реакцию и фиксируют цвета окрашенных клеток.
Инструкции по технике безопасности
При использовании дифениламина в процессе окраски бумаги раствором в воде следует соблюдать некоторые инструкции по технике безопасности. Это позволит избежать возможных повреждений и опасных ситуаций.
| Химические свойства | Физические характеристики | Экологические аспекты |
|---|---|---|
| Дифениламин — это амин, который является производным анилина и обладает кислотными свойствами. На воздухе его реакция с кислородом может привести к образованию нежелательных продуктов. | Дифениламин хорошо растворяется в воде и уксусной кислоте. Приливают около 0,5 г дифениламина в стакан с раствором 25% HCl. Затем помещают стеклянную палочку и перемешивают до полного растворения аминов. Загар, наблюдаемый в процессе растворения, свидетельствует о вхождении железа в реакцию. | Использование дифениламина и процесс его растворения требуют наблюдения основных принципов экологии и безопасности. При избытке аминов возможно образование трехвалентного железа, которое может оказывать вредное воздействие на окружающую среду и морскую экосистему. |
При подготовке раствора дифениламина необходимо соблюдать следующие инструкции:
- Приготовление раствора производится методом Винклера. Для этого приливают в мерную колбу 250 мл воды, добавляют 8 мл уксусной кислоты, а затем 10 мл раствора КМnО4. Всё хорошо перемешивают до образования раствора карбазола с интенсивной окраской.
- При использовании кислоты необходимо бережно обращаться с раствором, чтобы избежать возможных ожогов и пятна на коже, одежде и оборудовании. При необходимости использования кислоты рекомендуется надевать перчатки.
- Перед растворением дифениламина рекомендуется проветрить помещение или использовать специальные защитные маски, чтобы избежать вдыхания вредных паров и отравления.
- В процессе растворения дифениламина рекомендуется обращать внимание на образование пузырей и дыма, что может свидетельствовать о химической реакции. При наблюдении таких признаков следует прекратить использование и прохладить раствор.
- После окончания работы с дифениламином необходимо тщательно промыть места взаимодействия амина и кислоты водой, чтобы предотвратить возможные ожоги кожи.
Соблюдение инструкций по технике безопасности гарантирует безопасное использование дифениламина и предупреждает возможность возникновения опасных ситуаций в процессе окрашивания бумаги.
Видео:
Взаимодействие алюминия со щёлочью и водой
Взаимодействие алюминия со щёлочью и водой by him74ru 45,621 views 13 years ago 1 minute, 5 seconds