- Образование этилена в результате реакции с водой
- § 15 Физические и химические свойства алкенов
- Физические свойства алкенов
- Химические свойства алкенов
- Бромирование алкенов
- Оглавление
- Физические свойства
- Химические свойства
- Горение
- Присоединение воды
- Присоединение брома
- Полимеризация
- Обесцвечивание
- Реакции присоединения
- Реакция полимеризации
- Реакции окисления
- Вопросы и задания
- Практ 1
- Этилен продукт реакции с водой
- Свойства и условия реакции
- Физические свойства и структура этилена
- Видео:
- Люминол. Флуоресцеин. Тетракис(диметиламино)этилен. Хемилюминесценция. Химия – просто
Образование этилена в результате реакции с водой
Этилен, или этилен, является простым органическим соединением, состоящим из молекулы C2H4. Этилен широко используется в промышленности для производства пластиков, природного газа и других веществ. В этой статье мы рассмотрим, как этилен реагирует с водой и какие продукты образуются.
Когда этилен взаимодействует с водой, происходят как физические, так и химические реакции. В условиях наличия некоторых катализаторов, таких как бром или кислород, происходит полимеризация этилена. При этом этиленные молекулы присоединяются друг к другу, образуя полипропилен или другие полимеры.
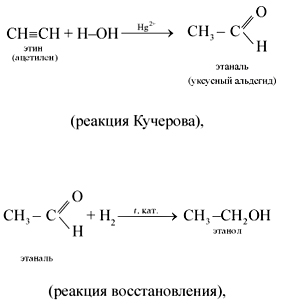
Водородное окисление этилена в присутствии катализатора также является одной из возможных реакций. Во время этой реакции молекула этилена присоединяет молекулу воды, и продуктом становится этанол. Это уравнение может быть представлено следующим образом:
C2H4 + H2O → C2H5OH
С другой стороны, взаимодействие этилена с атомами брома в водном растворе приводит к образованию 1,2-дибромэтана. Катализатором этой реакции может выступать KMnO4 или другие соединения, обладающие окислительными свойствами. Ниже приведено уравнение этой реакции:
C2H4 + Br2 → C2H4Br2
Таким образом, взаимодействие этилена с водой может приводить к различным реакциям, образующим различные продукты. Это явление широко изучается и используется в промышленности для производства различных химических соединений.
§ 15 Физические и химические свойства алкенов
Физические свойства алкенов
Алкены являются газообразными или жидкими веществами с низкими температурами кипения. За счет двойной связи, алкены имеют более высокую плотность и плотность паров, чем алканы с одинаковым числом углеродных звеньев. Они обычно слабо растворимы в воде, но хорошо растворяются в органических растворителях.
Алкены обладают свойствами двойной связи, такими как изомеризация и трансплантация. Изомеризация означает изменение расположения атомов в молекуле без изменения числа атомов или их связей. Трансплантация, с другой стороны, означает перемещение или перенос атомов или групп атомов в молекуле.
Химические свойства алкенов
Алкены имеют ряд характерных химических свойств, которые связаны с наличием двойной связи между атомами углерода.
Одним из основных химических свойств алкенов является их способность к аддиционным реакциям. Например, алкены могут образовывать аддукты с различными веществами, такими как водород, бром и калий перманганат (KMnO4). При вступлении брома в реакцию с этиленом, образуется бромэтилен или этиловый бромид. Реакция окисления алкенов с помощью KMnO4 приводит к образованию карбоновых кислот.
Алкены также могут быть подвержены полимеризации, в результате которой образуется полимерная пленка. Этот процесс обычно происходит при протекании реакции в присутствии каталитических агентов или при повышении температуры и давления.
Бромирование алкенов
Бромирование — это реакция алкенов с бромом. При контакте с бромной водой алкены образуют аналогичные бромэтаны (этиловый бромид). Эта реакция основана на аддиции брома к углеродной двойной связи. Реакция бромирования представляется следующим уравнением:
Реакция: C2H4 + Br2 = BrCH2CH2Br
Это уравнение показывает, что этилен (C2H4) присоединяет одну молекулу брома (Br2), образуя бромэтан (BrCH2CH2Br).
Протекание реакции бромирования можно легко различить благодаря изменению цвета реакционной смеси. Исходно фиолетовый раствор брома обесцвечивается под влиянием этилена.
Таким образом, физические и химические свойства алкенов являются важными для практического применения этих соединений. Изучение этих свойств позволяет более глубоко понять их реакционный характер и использовать их в различных сферах, таких как промышленность и медицина.
| Свойства | Описание |
|---|---|
| Физические свойства | Низкая температура кипения, низкая растворимость в воде, высокая плотность и плотность паров |
| Химические свойства | Аддиционные реакции, полимеризация, бромирование |
Оглавление
1. Введение
2. Этилен: свойства и присоединение воды
3. Реакция этилена с водой
3.1. Уравнение реакции
3.2. Химическое превращение этилена
3.3. Катализаторы реакции
4. Образование полипропилена
4.1. Мономерные связи в полимере
4.2. Процесс полимеризации
5. Реакции этилена с другими веществами
5.1. Бромирование этилена
5.2. Окисление этилена
5.3. Реакция этилена с водородом
6. Физические свойства и применение этилена
6.1. Способы получения этилена
6.2. Химические свойства этилена
6.3. Применение этилена в промышленности
7. Заключение
Физические свойства
Вода протекает в этилене через реакции с водородом, что образует этиленгликоль C2H4(OH)2.
Этилен также образуется в результате бромирования этилена и иодной пробой этилена. Таким образом, он может быть превращен в более длинные алкены с помощью реакций полимеризации или добавления.
Одним из основных физических свойств этилена является его способность проявлять светочувствительность при воздействии ультрафиолетовых лучей. Это свойство активно используется в производстве плёнки для пленочной фотографии.
Однако, хотя этилен и оказывает сопротивление окисления нескольких мономерных звеньев полимера, он сам реагирует с бромным водным раствором, образуя гомополимер поливинилбромида. Для различить число двойных связей этилена можно использовать некоторые реакции, такие как бромирование и присоединение Хофмана.
Химические свойства
Этилен обладает рядом химических свойств, которые делают его важным продуктом реакции с водой.
Горение
Этилен является горючим газом. При горении этилена с воздухом образуется углекислый газ и вода:
C2H4 + 3O2 → 2CO2 + 2H2O
Эти химические реакции особенно важны для получения энергии.
Присоединение воды
Этилен может присоединяться к воде и образовывать этанол:
C2H4 + H2O → C2H5OH
Это реакция полусуммаризации, в которой две молекулы этилена превращаются в одну молекулу этанола. Присоединение воды к этилену происходит при нагревании в присутствии катализатора.
Присоединение брома
Этилен может присоединяться к брому и образовывать бромэтилан:
C2H4 + Br2 → C2H4Br2
Эта реакция протекает легко при комнатной температуре без катализатора.
Образование этого бромэтана является качественной реакцией для этилена.
Полимеризация
Этилен может подвергаться полимеризации — реакции, в результате которой образуется полимер. При полимеризации этилену образуется полипропилен — широко используемый пластиковый материал:
(C2H4)n → [-CH2-CH2-CH2-…-CH2-CH2-]n
Процесс полимеризации происходит при присутствии катализаторов и специальных условий.
Обесцвечивание
Этилен может использоваться для обесцвечивания определенных веществ. Он может прореагировать с KMnO4 и привести к уменьшению интенсивности фиолетового цвета раствора:
C2H4 + KMnO4 → C2H4O + MnO2
Таким образом, этен играет роль в качественной реакции для определения наличия природных соединений.
Реакции присоединения
Одной из простейших и наиболее практически значимых реакций присоединения является реакция этилена с водой. При этом образуется этиленгликоль (этанола), который широко используется в промышленности для производства пластиков, полимеров, пленок и других материалов. Уравнение реакции присоединения этилена и воды можно записать следующим образом:
C2H4 + H2O → C2H6O
Если в течение реакции присоединения через раствор хлористого водорода пропустить газы, то произойдет бромирование этилена. При этом образуются соединения, являющиеся бромпроизводными этана. Реакция бромирования этилена представлена следующим уравнением:
C2H4 + Br2 → C2H4Br2
Также этилен может реагировать с бромом при нагревании в условиях отсутствия света. В результате образуются твердые соединения, которые используются в медицине для образования плёнки, применяемой при обесцвечивании кожи.
Кроме того, этилен может реагировать с растворами кислорода и калия перманганата (KMnO4) при пониженной температуре. При этом происходит окисление этилена, и образуются полиоксиметилены, которые затем используются в качестве пластификаторов в производстве пластиков.
Реакция полимеризации
Этилен (C2H4) — это газообразное соединение, содержащее две двойные связи между атомами углерода. Он широко используется в промышленности для производства различных полимерных материалов, таких как пленка, пластик и волокна.
Реакция полимеризации этилена происходит при наличии катализатора и осуществляется под воздействием физических условий, таких как высокая температура и давление.
Протекание реакции полимеризации можно представить следующим уравнением:
C2H4 + C2H4 + … → (C2H4)n
Где (C2H4)n — это полимер, состоящий из числа мономерных единиц этилена.
Во время реакции полимеризации каждая молекула этилена присоединяется к другой молекуле этилена, образуя длинную цепь полимера. Этот процесс протекает через образование иодной связи между мономерными единицами этилена.
Реакция полимеризации идет со значительным выделением тепла, что является общим свойством таких реакций. Кроме того, полимеризация этилена происходит при приведении воды, что приводит к обесцвечиванию фиолетового раствора брома и образованию бромного раствора.
Реакция полимеризации этилена является очень важным явлением, так как позволяет получать полимерные материалы с различными физическими и химическими свойствами. Полимеры, полученные в результате полимеризации этилена, используются во многих областях промышленности, включая производство пластиковых изделий, упаковки, изоляционных материалов и других продуктов.
Реакции окисления
2C2H4 + 3O2 → 4CO2 + 4H2O
Таким образом, продуктами горения этилена являются углекислый газ и вода.
Этанол, молекула которого содержит одну двойную связь, может претерпевать реакцию окисления с помощью некоторых химических реагентов. Например, окисление этанола с помощью KMnO4 приводит к образованию ацетата калия. Эта реакция может быть использована, например, для обесцвечивания фиолетового раствора KMnO4.
Реакции окисления этилена могут быть также использованы для получения полипропилена или других полимеров. Например, при полимеризации этилена с помощью специального катализатора и при определенных условиях протекает реакция присоединения молекул этилена друг к другу, что приводит к образованию длинных цепей полимера. Этот процесс можно описать следующим уравнением:
nC2H4 → [-C2H4-]n
Таким образом, продуктом полимеризации этилена является молекулярный полипропилен, состоящий из повторяющихся звеньев этилена.
Вопросы и задания
1. Что такое этилен и какой у него состав и свойства?
Этилен — это безцветный газ, состоящий из двух атомов углерода и четырех атомов водорода. У него есть ряд физических и химических свойств, таких как низкая плотность, нерастворимость в воде, различимый запах, хорошая горючесть и др.
2. Как этилен реагирует с водой и как можно различить эту реакцию?
Этилен реагирует с водой при наличии катализатора (например, сульфованадиевой кислоты) и образует этиленгликоль — химическое соединение, используемое в промышленности. Реакцию можно различить по образованию облачка пара над местом смешения газа с водой.
3. Какой вид протекает реакции бромирования этилена в водном растворе?
Водные растворы брома обесцвечиваются при протекании реакции бромирования этилена. Это происходит из-за образования бромсодержащих соединений, которые не обладают окраской.
4. Как происходит реакция окисления этилена?
Реакция окисления этилена может протекать при нагревании под воздействием кислорода или водными растворами перманганата калия. В результате образуется двухатомная молекула углекислого газа и вода.
5. Какие химические свойства имеют алкены по сравнению с алканами?
Алкены обладают рядом химических свойств, которые отличают их от алканов. Например, они могут претерпевать реакции присоединения, окисления и полимеризации благодаря наличию двойной связи между атомами углерода в их молекуле.
6. Для чего используется этилен в промышленности?
Этилен широко используется в промышленности для получения полимерных материалов. Он служит исходным веществом для синтеза полиэтилена и других пластмасс, которые имеют широкое применение в различных отраслях.
Дайте краткий ответ на вопросы:
1. Какие свойства имеет этилен?
Этилен — безцветный газ с хорошей горючестью, нерастворимый в воде, различимого запаха.
2. Как реагирует этилен с водой?
Этилен с водой реагирует при наличии катализатора, образуется этиленгликоль.
3. Что происходит при бромировании этилена в водном растворе?
Водные растворы брома обесцвечиваются, образуются бромсодержащие соединения.
4. Как происходит реакция окисления этилена?
При окислении этилена образуется углекислый газ и вода.
5. Какие особенности имеют алкены по сравнению с алканами?
Алкены активнее претерпевают реакции присоединения, окисления и полимеризации благодаря наличию двойной связи в молекуле.
6. Для чего используется этилен в промышленности?
Этилен используется для получения полимерных материалов, таких как полиэтилен и пластмассы.
Расшифруйте формулу:
1. Бр + Эт =>
Бром + этилен -> этиленбромид.
Практ 1
Протекание реакции происходит через промежуточные звенья полимера этена, что позволяет различить число звеньев в молекуле продукта.
Этанол – основной продукт качественной реакции окисления этена под влиянием катализатора. Этиловый спирт обладает рядом полезных свойств и широко используется в различных отраслях промышленности.
Одной из вариантов реакции этилена с водой является образование алканов и алкенов. Бромная вода присоединяет к двойной связи молекулы этена и соединяет атомы водорода и углерода, тем самым обесцвечивая фиолетовый раствор брома. Уравнение реакции:
СН2=СН2 + H2O → СН3-СН2-ОН
В ходе реакции происходит полимеризация этилена, благодаря которому образуется большое число мономерных звеньев полимера. Этилену свойственна легкая полимеризация, что делает его важным компонентом в производстве различных полимерных материалов.
Процесс реакции этилена с водой можно пронаблюдать при помощи качественной реакции с калия перманганатом (KMnO4), которая дает следующие результаты:
- Фиолетовый раствор KMnO4 обесцвечивается в результате окисления этанола.
- Образуется белый осадок оксида марганца (IV) (MnO2).
- Происходит выделение пузырьков газа – это кислород, освобождающийся в процессе горения
Таким образом, реакция этилена с водой является важным явлением в органической химии и имеет широкое применение в промышленности.
Этилен продукт реакции с водой
Свойства и условия реакции
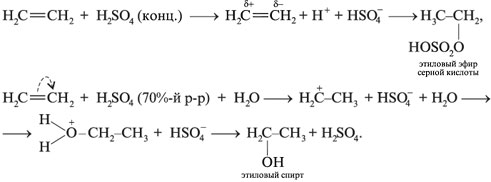
Реакция присоединения этена к воде протекает при наличии катализатора, который обычно служит серная кислота. В результате этой реакции образуются практологие растворы этанола, которые могут образовывать плёнку на поверхности воды.
Этилен образует более 15 различных продуктов при присоединении к воде. Главным продуктом реакции является этанол, однако могут образовываться и другие соединения, такие как пропанол и иногда этиленгликоль. Реакция присоединения также может приводить к образованию полимеров, таких как полипропилен.
Физические свойства и структура этилена
Этилен представляет собой газ, который хорошо растворяется в воде, образуя слабые водородные связи с молекулами воды. Молекула этена состоит из двух углеродных атомов, соединенных двойной связью, и четырех атомов водорода.
Этилен — один из наиболее важных промышленных химических соединений, который используется в производстве пластмасс, резиновых изделий и других материалов. Этилен также находит применение в процессах синтеза органических соединений и в производстве пестицидов и удобрений.
Видео:
Люминол. Флуоресцеин. Тетракис(диметиламино)этилен. Хемилюминесценция. Химия – просто
Люминол. Флуоресцеин. Тетракис(диметиламино)этилен. Хемилюминесценция. Химия – просто by Химия – Просто 55,321 views 7 years ago 7 minutes, 6 seconds