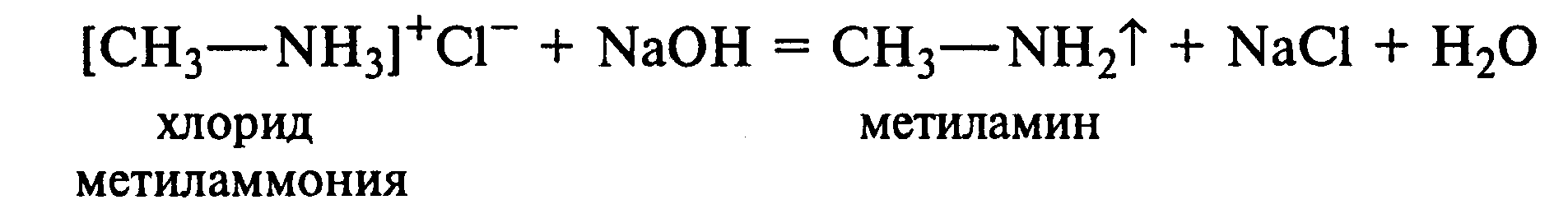- Свойства и применение хлорида метиламмония в реакции с водой
- Амины
- Хлорид метиламмония
- Строение
- Получение и характеристики
- Использование
- Оглавление
- Извлечение и представление
- Характеристики
- Использование хлорида метиламмония с водой
- Изомерия
- Взаимодействие с другими соединениями
- Задания для подготовки к ЕГЭ на амины
- Утверждение 1:
- Утверждение 2:
- Амины Тестовые задания с выбором двух вариантов ответа
- Видео:
- Сделал ВЕЧНЫЕ ЛИСТЬЯ Из Никеля! Гальванотехника.
Свойства и применение хлорида метиламмония в реакции с водой
Хлорид метиламмония (CH3NH3Cl) является молекулярным соединением, которое образуется в результате взаимодействия метиламина с хлороводородной кислотой. Он представляет собой белое кристаллическое вещество с характерным запахом аммония.
Хлорид метиламмония широко используется в химической промышленности и научных исследованиях. Он является важным промежуточным продуктом для производства различных органических соединений. Также он находит применение в фармацевтической промышленности, в процессе добавления к хлоркалиевым солям для нивелировки экстракции фенола, и в других химических процессах.
Взаимодействие хлорида метиламмония с водой приводит к образованию метиламина и хлороводорода. Это реакция обратима и может протекать в обе стороны в зависимости от условий. При обычных условиях, хлорид метиламмония легко растворяется в воде, а его раствор имеет слабую щелочную окраску.
Амины
Амины классифицируются в зависимости от числа замещенных атомов водорода на атом азота. Так, первичные амины имеют одну замещенную группу, вторичные — две, а третичные — три.
Одной из характеристик аминов является их щелочная природа. Благодаря наличию аминогруппы амины могут вступать в реакцию с кислотами, образуя соли. Например, этиламин (С2Н5NH2) может реагировать с хлоридом гидрогена (HCl) и образовывать хлорид этиламмония (C2H5NH3Cl).
Ароматические амины также могут проявлять характеристики ароматических соединений, что связано с наличием ароматических ядер в их структуре.
Хлорид метиламмония
Строение
Молекулярное строение хлорида метиламмония представляет собой триметиламин, в котором один атом водорода замещен хлором. Таким образом, формула соединения становится NH3CH3Cl.
Получение и характеристики
Хлорид метиламмония получают путем реакции метиламина (NH2CH3) с хлоридом водорода (HCl) при нормальных условиях. Результатом реакции является образование твердого вещества, представленного в виде белых кристаллических гранул. Хлорид метиламмония легко растворяется в воде и образует кислую среду. Он также может быть получен путем извлечения хлорида метиламмония из органических соединений с использованием натрия (NaOH) и нитрозоуксусной кислоты (HNO2).
Использование
Хлорид метиламмония относится к классу группы газа, азотистыми соединениями и ароматическим веществам. Используется в химической промышленности для получения органических соединений, таких как молекулярные изомеры и другие сложные вещества. Хлорид метиламмония также может быть использован в качестве тестового реагента для определения присутствия молекулярного азота в органических соединениях.
Оглавление
- Введение
- Описание хлорида метиламмония
- Взаимодействие хлорида метиламмония с водой
- Реакция между хлоридом метиламмония и водой
- Образование аминогруппы в результате взаимодействия
- Образование первичных, вторичных и третичных алкиламмонийных гидрохлоридов
- Окраска растворов хлорида метиламмония с водой
- Мольное соотношение хлорида метиламмония и воды
- Классгруппа алкиламмонийных гидрохлоридов
- Описание реакции взаимодействия этиламина с хлоридом метиламмония
- Реакция образования искомого продукта
- Свойства и применение хлорида метиламмония
- Заключение
Извлечение и представление
Процесс извлечения и представления хлорида метиламмония с водой включает в себя несколько этапов. Первоначально, хлорид метиламмония растворяется в воде, а затем добавляется предполагаемое количество азотистой кислоты. В результате образуется гидрохлорид метиламмония. В ходе данной реакции образуются следующие продукты: соединение, обозначенное как продукт, которое образовалось в результате реакции между хлоридом метиламмония и водой.
Третичные аминогруппы, такие как этиламин и диэтиламина, вступают в реакцию с хлоридом метиламмония и образуют соединение, обозначенное как продукт реакции. Растворимость гидрохлорида метиламмония в воде зависит от оксидационного состояния азота.
Структура и свойства гидрохлорида метиламмония можно представить следующим образом: гидрохлорид метиламмония — это соль, в которой положительный ион (метиламмоний) содержит азот и водород, а отрицательный ион (хлорид) содержит хлор. Оба иона имеют свои уникальные химические и физические характеристики.
Для извлечения и представления гидрохлорида метиламмония с водой можно использовать таблицу химических свойств и структуру данного вещества. Гидрохлорид метиламмония обладает сложной органической структурой, поэтому его характеристики могут быть обозначены в виде формулы и систематического названия.
Окраска гидрохлорида метиламмония в водном растворе может служить индикатором его состояния. Обычно раствор гидрохлорида метиламмония имеет прозрачную или слегка желтоватую окраску, но при повышенной концентрации или при добавлении других реактивов окраска может измениться.
Таким образом, извлечение и представление гидрохлорида метиламмония с водой требует использования специальных реактивов и методов. Полученные данные могут быть использованы для дальнейшего изучения химических свойств и возможных применений данного соединения в органической химии.
Характеристики
Взаимодействуя с водой, хлорид метиламмония образует раствор, который является кислотным. Под воздействием основания, например натрия гидроксида (NaOH), в данной стадии может происходить превращение в соответствующие ароматические аминогруппы.
К характеристикам хлорида метиламмония можно отнести также его свойство взаимодействовать с лакмусовой бумагой, измерять рН среды, и представлять собой реактив, который может быть использован в химических анализаторах.
Аминогруппа в хлориде метиламмония является первичным амином. Классификация алкиламмония подразумевает, что образование вторичного амина может произойти за счет подбирания амииака к первичному амину при соответствующих условиях в растворах кальция и бария.
Ароматический фенол также относится к органическим соединениям. В отличие от хлорида метиламмония, фенол обладает алифатической структурой. Изомерия вещества может быть выражена в разных положениях аминогруппы и метильной группы в молекулярной структуре. Например, хлорид метиламмония может обозначаться как NH2CH2COOH или NH2CH2COOH. Подберите соответствующие позиции аминогруппы и метильной группы с помощью букв V и M
Количество соединений с классгруппой аминов огромно, и их молекулярная сложность может быть выражена в разных структурах. Хлорид метиламмония представляет собой одно из таких соединений с реактивными свойствами, которые могут быть использованы в различных химических реакциях.
Использование хлорида метиламмония с водой
Хлорид метиламмония можно использовать в ряде реакций. Одна из таких реакций — взаимодействие хлорида метиламмония с водой. В результате этой реакции образуется метиламин (CH3NH2) и соляная кислота (HCl).
Метиламин (CH3NH2) является первичным амином, так как в его молекуле только одна аминогруппа. Этот органический заместитель относится к классу амина. Химические характеристики метиламина соответствуют первичным аминам.
Вода (H2O) является простейшей веществом и характеризуется молекулярной формулой H2O. Вода может вступать в реакцию с различными соединениями и веществами, в том числе и с хлоридом метиламмония.
Для взаимодействия хлорида метиламмония с водой могут быть выбраны следующие условия: реакционная смесь содержит хлорид метиламмония и воду, соотношение компонентов обозначено К (NH4Cl : H2O), и взаимодействие происходит при комнатной температуре и атмосферном давлении.
Данная реакция может быть предположена на основе знания характеристик хлорида метиламмония и воды, а также в соответствии с классом аминов. Результатом взаимодействия хлорида метиламмония с водой является образование метиламина и соляной кислоты.
| Вещество | Молекулярная формула | Характеристики |
|---|---|---|
| Хлорид метиламмония | NH4Cl | Соль органического амина |
| Метиламин | CH3NH2 | Превратиться в соляную кислоту (HCl) |
| Вода | H2O | Вступает в реакцию с хлоридом метиламмония |
Изомерия
Метиламин имеет только одну возможную структуру, поэтому изомерия не возникает.
Взаимодействие с другими соединениями
Метиламин может взаимодействовать с другими соединениями, такими как воздух, кислород, амины, фенол и другие органические соединения. Реакций метиламина с такими соединениями может быть несколько в зависимости от условий и выбранного реактива.
Задания для подготовки к ЕГЭ на амины
Амины представляют собой класс соединений, которые обладают характеристиками как оснований, так и нуклеофилов. Учащимся необходимо знать названия и формулы нескольких аминов, а также уметь проводить реакции их с другими веществами.
Для начала, предлагается установить, какие из следующих утверждений об аминах и их свойствах верны:
Утверждение 1:
Амины могут выступать в качестве кислот или оснований, в зависимости от условий реакции. Это связано с наличием в их строении аминогруппы (-NH2).
Утверждение 2:
Амины могут быть классифицированы по типу аминогруппы и количеству аминогрупп в молекуле.
Ответы:
- Для установления истинности каждого утверждения, необходимо привести примеры аминов и их реакций.
- Исходные вещества для проведения экспериментов можно использовать те, которые были рассмотрены в предыдущих разделах данной статьи.
- При проведении реакции можно использовать следующие реагенты: хлорид метиламмония (CH3NH3Cl), вода (H2O), HNO3, HNO2, CH3NH2, соль NH4Cl, CH3NH3HCO3, лакмусовый барий, фенол, этиламин, NaCO2, V(CO)2(V2M-лакмус, V2V-MB2).
Продукт реакции амина с хлоридом метиламмония и водой можно обозначить следующей формулой: MH2O+MH2O. Для определения продуктов такой реакции необходимо провести соответствующие эксперименты.
Амины классифицируются по типу аминогруппы и количеству аминогрупп в молекуле:
- Амин M — основание сложности взаимодействия соединения M с реагентом V(CO)2(V2M-лакмус) и лакмусовым барием, а также с веществом V(CO)2(V2V-MB2)
- Амин N — основание схожее с алкалинами, но легче соединяемое с ароматическими соединениями
- Амин P — простейшая соль NH4Cl
Таким образом, верными являются оба утверждения 1 и 2. Необходимо запомнить, что амины могут быть представлены разными классами соединений, взаимодействие с которыми может иметь различные характеристики.
Амины Тестовые задания с выбором двух вариантов ответа
Перед вами представлены тестовые задания, в которых нужно выбрать один из двух вариантов ответа, соответствующий условиям задания. Для выбора правильного ответа запишите букву, соответствующую этому варианту.
| Вопрос | Варианты ответа |
|---|---|
| 1. Какое вещество растворимо в воде? | a) Триметиламин b) Метиламин |
| 2. Какая классгруппа аминов представлена формулой (CH3)3N? | a) Первичные b) Третичные |
| 3. Какая аминогруппу содержит алкиламмоний? | a) NH2 b) NH3 |
| 4. Какой продукт превращения аммиака при реакции с хлоридом метиламмония в водных условиях? | a) H3C-NH3Cl b) NH3Cl |
| 5. Какие характеристики соответствуют ароматическим аминам? | a) Очень сложные реакции b) Хорошая растворимость в спирте |
| 6. Какое количество этиламина содержит соединение представленное формулой C2H5NH2? | a) 1 b) 2 |
| 7. Какое вещество окрашивает реакция ароматических аминов с нитритами калия? | a) Красным b) Белым |
| 8. Какая аминогруппу содержит тригинидриловый амина? | a) -NH2 b) -NHNH2 |
| 9. Какие продукты образуются при взаимодействии метиламином с кислотой? | a) NNMn b) NNH2 |
| 10. Какие основания сильнее находятся в ряду: метиламоний, анилин, хлорид метиламмония? | a) Хлорид метиламмония b) Анилин |
Могут быть задания другой сложности, поэтому внимательно читайте условия и выбирайте правильный ответ.
Видео:
Сделал ВЕЧНЫЕ ЛИСТЬЯ Из Никеля! Гальванотехника.
Сделал ВЕЧНЫЕ ЛИСТЬЯ Из Никеля! Гальванотехника. by Thoisoi 1,078,795 views 4 years ago 18 minutes