- Как использовать олеиновую кислоту и перманганат калия для очистки воды
- Свойства олеиновой кислоты
- Реакция с перманганатом калия
- Окисление и горение
- Мылообразование
- 62 Свойства олеиновой кислоты
- 1. Физические свойства
- 2. Химические свойства
- 3. Реакция с перманганатом калия
- Реакции окисления
- Изомеризация олеиновой кислоты в элаидиновую
- 63 Окисление жиров и масел Реакция Вагнера
- 7 Амины
- Способы получения аминов:
- Свойства аминов:
- Примеры аминов:
- 71 Получение этиламина
- 72 Свойства аминов
- Методичка по органике Методические указания по выполнению лабораторных работ по курсу Органическая химия
- Описание лабораторной работы
- Необходимое оборудование
- Метод выполнения
- Ожидаемый результат
- Важные указания
- Видео:
- СОЖ для заточки ножей? Осторожно, олеиновая кислота.
Как использовать олеиновую кислоту и перманганат калия для очистки воды
Олеиновая кислота – одна из основных жирных кислот, которая является незаменимым компонентом многих продуктов и материалов. Она обладает уникальными свойствами и широко используется в различных областях, включая пищевую, медицинскую и химическую промышленность. Олеиновая кислота является жирной кислотой, образующей глицериловую олеиновую кислоту в процессе омыления жиров и масел.
Олеиновая кислота примечательна своей способностью образовывать соли, эфиры и амиды. В данном опыте будет исследована реакция олеиновой кислоты с перманганатом калия в присутствии воды. Для этого необходимо приготовить раствор калия и разлить по пробиркам. Затем в каждую пробирку добавляют немного олеиновой кислоты и наблюдают за происходящей реакцией.
Процесс образования перманганата калия в присутствии олеиновой кислоты представляет собой химическую реакцию окисления. При нагревании раствора происходит окисление кислоты между перехода цвета перманганата из фиолетового в голубоватые оттенки. Этот опыт является качественным методом определения присутствия олеиновой кислоты и ее реакционных свойств.
Свойства олеиновой кислоты
Реакция с перманганатом калия
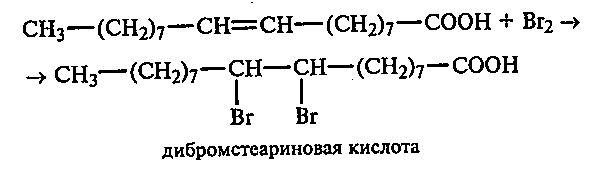
Олеиновая кислота реагирует с перманганатом калия в присутствии воды. При добавлении перманганата калия в раствор олеиновой кислоты, раствор окрашивается в фиолетовый цвет. Это свидетельствует о наличии двойных связей в структуре кислоты.
Окисление и горение
Олеиновая кислота может быть подвержена окислению. При нагревании олеиновой кислоты в кислой среде, она может образовывать элаидиновую кислоту – вторичный продукт окисления. При нагревании олеиновая кислота может гореть с ярким пламенем и выделять углекислый газ.
Мылообразование
Олеиновая кислота может быть использована для производства мыла. Она реагирует с щелочами, такими как гидроксид натрия или гидроксид калия, образуя натриевую или калиевую соль олеиновой кислоты. Этот процесс называется мылообразованием.
| Свойство | Описание |
|---|---|
| Элаидиновая кислота | Это вторичный продукт окисления олеиновой кислоты |
| Окрашивание перманганатом калия | Олеиновая кислота окрашивается в фиолетовый цвет при взаимодействии с перманганатом калия |
| Горение | Олеиновая кислота может гореть с ярким пламенем и выделять углекислый газ |
| Мылообразование | Олеиновая кислота может быть использована для производства мыла |
62 Свойства олеиновой кислоты
1. Физические свойства
Олеиновая кислота представляет собой безцветную или слабо-желтоватую жидкость. Ее плотность составляет примерно 0,89 г/см³ при 25°C. Олеиновая кислота практически не растворима в воде, но хорошо смешивается с органическими растворителями, такими как спирт и масла.
2. Химические свойства
Содержимое олеиновой кислоты в бане под воздействием хлоридом серебра окрашивается в темно-серый цвет, указывая на присутствие двойной связи в молекуле. Поэтому олеиновая кислота является ненасыщенной жирной кислотой.
Олеиновая кислота образует смесь с муравьиной, уксусной и салициловой кислотами, а также с этиловым спиртом. При нагревании олеиновой кислоты с хлоридом бария образуется баритовая соль. Олеиновая кислота взаимодействует с моносахаридами и образует продукты окисления.
При окислении олеиновой кислоты образуются продукты смешанного состава, включая уксуснокислый ангидрид и оксиды высших углеродных кислот.
3. Реакция с перманганатом калия
Олеиновая кислота реагирует с перманганатом калия при нагревании, что вызывает окрашивание смеси в фиолетовый цвет. Смесь при этом выделяет тепло и горит с вспышками. Реакция окисления олеиновой кислоты с перманганатом калия является одним из классических заданий на курсе химии.
Эти свойства олеиновой кислоты являются основными и часто используются в лабораторных работах и исследованиях.
Реакции окисления
Перманганат калия — металлическое соединение, которое широко применяется в химических экспериментах. При взаимодействии с олеиновой кислотой в присутствии воды, происходит окисление кислоты. Результатом реакции является образование осадка — черного масла. Эта реакция можно наблюдать, если в пробирку добавить несколько капель перманганата калия, затем добавить каплю олеиновой кислоты и нагреть смесь. При этом, цвет перманганата калия меняется с фиолетового на коричневый, а затем на черный.
Еще одним примером реакции окисления является реакция моносахаридов с хлоридом меди(II) в присутствии уксуснокислой кислоты. При взаимодействии моносахаридов с хлоридом меди(II) в растворе уксуснокислой кислоты происходит окисление моносахаридов. Результатом реакции является образование осадка медного оксида, выделяющегося в виде черного цвета.
Одним из методов омыления масла является реакция окисления. При этом, масло нагревают в присутствии водного раствора перманганата калия, в результате чего оно окисляется и образуется олеиновая кислота.
Кроме того, в органической химии широко применяется реакция окисления вторичных аминов. Одним из примеров такой реакции является окисление уксусной кислоты с помощью перманганата калия. Результатом реакции является образование салициловой кислоты.
Таким образом, реакции окисления имеют большое значение в химии. Они позволяют получать новые вещества с измененными свойствами и составом. Эти реакции происходят в присутствии окислителя, таким как перманганат калия, и могут быть различными в зависимости от условий проведения эксперимента.
Изомеризация олеиновой кислоты в элаидиновую
В ходе реакции изомеризации олеиновой кислоты в элаидиновую используется перманганат калия в воде. Эта реакция основывается на окислении двойных связей в олеиновой кислоте электрофильным перманганатом калия.
Для проведения эксперимента, в пробирку добавляют одну часть олеиновой кислоты и две части воды. Затем приливают раствор перманганата калия, предварительно разведенный в воде, примерно к концу проведения эксперимента. В результате окисления олеиновой кислоты образуется элаидиновая кислота. Следует отметить, что в процессе реакции содержимое пробирки окрашивается в голубоватые тона из-за образования галловой кислоты и муравьиной кислоты в результате окисления.
При окислении олеиновой кислоты с использованием перманганата калия также выделяется осадок, состоящий из медных солей. Указания на пробирках и методичка по органической химии могут включать также внесение щелочной соли, которая предварительно продиссоциируется с оксидом уксусной кислоты. Это позволяет совсем избавиться от медного осадка, а также избежать его появления в ходе окисления происходит долгий прилив бромной воды. Затем содержимое пробирки слегка нейтрализуют гидроксидом натра, а затем доба- вляют недостающую соль натра. Процесс изоме- ризации олеиновой кислоты в элаидиновую продолжается довольно долго, медленно и слежными бульканиями выделяющийся газ с пропионовым запахом. В холодной жидкости не растворя- ется и хорошо отделяется; элаидиновая кислота в отличие от олеиновой окисляется перманга- ната.
63 Окисление жиров и масел Реакция Вагнера
Для проведения реакции Вагнера необходимо нагреть пробирку с альдозом и добавить к нему несколько капель раствора перманганата калия. Затем пробирка нагревается над пламенем до образования элаидиновой кислоты. При этом, в результате окисления линолевой кислоты, капля перманганата калия окрашивается в зеленый цвет.
Окисление жиров и масел при обработке перманганатом калия является достаточно энергичной реакцией. Для предотвращения образования однородных растворов с перманганатом калия, используют щавелевую или уксусную кислоту. Натрий или калий перманганат взаимодействуют с кислотами или их солями, образуя цветные оксиды со знакомым свойством высшей окислительной способности в лабораторных работах.
Реакция Вагнера является одной из важных реакций для определения масел и жиров в курсе аналитической химии. Она может применяться для определения цветных веществ в растворах галловой и уксусной кислот, состава карбоновых кислот и карбоциклических соединений, а также для получения оксидов по методу Вагнера.
Реакция Вагнера может проводиться не только с перманганатом калия, но и с другими оксидами, например, с черным щавелевым или медным окисью. Сравнение цвета образовавшихся осадков или растворов позволяет определить наличие или отсутствие определенного иона в растворе.
Для проведения реакции Вагнера необходимо оборудование: пробирка, проволока, горелка или пламя, масло, растворы перманганата калия, щавелевой или уксусной кислоты.
В результате реакции Вагнера происходит окисление альдозов и образование окисей моносахаридов. Нагретая смесь альдоза и перманганата калия окрашивается в фиолетовый цвет, в то время как нагретый натр щелочи с щавелевой кислотой образует разветвленную свечу с высокой концентрацией натрия и галловой кислоты.
Таким образом, реакция Вагнера играет важную роль в процессе окисления жиров и масел. Она может быть использована для получения различных оксидов, а также для определения наличия или отсутствия определенных ионов в растворе.
7 Амины
Способы получения аминов:
1. В качестве исходных соединений могут использоваться алкилгалогенпроизводные, а также некоторые другие органические соединения, содержащие функциональные группы, способные к протеканию разнообразных химических реакций.
2. Одним из наиболее распространенных методов получения аминов является амонолиз, который проводят путем обработки соответствующих галогеналканов аммиаком при нагревании с образованием аминов и солей аммония.
Свойства аминов:
— Воспламеняются на воздухе и сгорают с ярким пламенем;
— Проявляют свойства оснований и реагируют с кислотами;
— Встречаются в природе в составе многих биологических соединений;
— Обладают специфическим ароматом;
— Имеют выраженную аминную реакцию, характеризуемую образованием осадка с глюконовыми солями меди.
Примеры аминов:
| Наименование | Структурная формула |
|---|---|
| Метиламин | NH2CH3 |
| Этиламин | NH2C2H5 |
| Триметиламин | (CH3)3N |
71 Получение этиламина
72 Свойства аминов
Одним из свойств аминов является их реакция с перманганатом калия в присутствии щавелевой или олеиновой кислоты. При такой реакции появляется фиолетовая окрашенная реакционная жидкость.
Амины также могут подвергаться окислению, например, при воздействии перманганата калия или окисления глюкозы. При этом образуются продукты окисления, такие как элаидиновая кислота или глюкоза.
Амины проявляют свойства щелочной натуре, поэтому они могут реагировать с кислотами и образовывать соли. Также, амины ведут себя как основания и могут реагировать с гидроксидами, образуя соли аммония.
Для выполнения реакций аминов с перманганатом калия или оксидацией глюкозы рекомендуется использовать методические указания:
| № | Описание реакции | Условия проведения |
|---|---|---|
| 1 | Окисление аминов перманганатом калия | Раствор амина и перманганата калия |
| 2 | Окисление аминов глюкозой | Раствор амина и глюкозы |
Также, несколько примеров реакций аминов могут быть проведены с использованием щелочи или уксуснокислого раствора. Например, на пробирку с амином приливают каплю щелочи и наблюдают за изменением цвета. При реакции с уксуснокислым раствором образуется фиолетовая окрашенная жидкость.
Методичка по органике Методические указания по выполнению лабораторных работ по курсу Органическая химия
Описание лабораторной работы
Лабораторная работа предназначена для изучения свойств олеиновой кислоты путем реакции перманганатом калия в водной среде. Олеиновая кислота, являющаяся карбоксильной кислотой, обладает важными химическими свойствами, которые могут быть изучены путем воздействия сильного окислителя, такого как перманганат калия.
Необходимое оборудование
Для выполнения лабораторной работы требуется следующее оборудование:
- Газоотводная колба.
- Пипетки для измерения капель.
- Химические реактивы: олеиновая кислота, перманганат калия, вода, серная кислота, этиловый спирт, этиламин, фенолфталеин.
- Стеклянные пробирки и мерные колбы.
Метод выполнения
1. В газоотводную колбу внесите 1 мл олеиновой кислоты и 20 мл воды.
2. К полученной смеси добавьте несколько капель перманганата калия.
3. Содержимое колбы аккуратно и энергично перемешайте до полного окрашивания раствора. При этом образуется осадок карбоновых кислот.
4. К полученной смеси добавьте концентрированную серную кислоту. При этом происходит окисление олеиновой кислоты до моносахаридов и образуется серный осадок.
5. При добавлении фенолфталеина к полученной смеси она окрашивается в розовый цвет. Далее, нагревайте смесь в бане до полного омыления. Под влиянием действия перманганата калия олеиновая кислота окисляется до уксуснокислого этиламина.
6. Проведите обратное превращение уксуснокислого этиламина в олеиновую кислоту с помощью внесения бромной воды. При этом появляется осадок бромида и бромной воды, а также выделяется бромоводород.
7. Изучите свойства полученного осадка, например, проведите реакцию с реагентами для обнаружения присутствия кислоты, аминов и медных ионов.
Ожидаемый результат
При проведении лабораторной работы можно ожидать следующие результаты:
- Оксид олеиновой кислоты действует на перманганат калия, окрашивая раствор в розовый цвет.
- При нагревании смесь оксидов олеиновой кислоты с этиловым спиртом и этиламином происходит образование осадка бромида, бромной воды и выделение бромоводорода.
- Осадок после добавления реагентов для обнаружения кислот, аминов и медных ионов может указывать на присутствие соответствующих соединений.
Важные указания
При выполнении лабораторной работы обратите внимание на следующие моменты:
- Олеиновая кислота является веществом, обладающим высокой реакционной способностью, поэтому работайте с ней осторожно, соблюдая все правила безопасности.
- Не вносите вещества в больших количествах, достаточно добавлять их по каплям.
- При нагревании смеси с этиловым спиртом и этиламином будьте осторожны из-за выделения едкого газа.
- Полученный осадок можно анализировать с использованием реагентов для обнаружения кислот, аминов и медных ионов.
| Вещества | Реагенты | Наблюдения |
|---|---|---|
| Олеиновая кислота | Перманганат калия | Раствор окрашивается в розовый цвет. |
| Оксиды олеиновой кислоты | Этиловый спирт, этиламин | Появляется осадок бромида, бромной воды, выделяется бромоводород. |
| Оксиды олеиновой кислоты | Реагенты для обнаружения кислот, аминов и медных ионов | Появляется осадок, свидетельствующий о наличии соответствующих соединений. |
Видео:
СОЖ для заточки ножей? Осторожно, олеиновая кислота.
СОЖ для заточки ножей? Осторожно, олеиновая кислота. by Valeriy Dnipro 3,272 views 1 year ago 9 minutes, 55 seconds