- Как называется процесс взаимодействия растворимого вещества с водой?
- Понятие о растворах Растворимость веществ
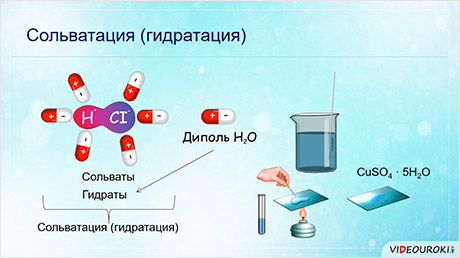
- Сольватация и гидратация
- Растворы насыщенные, ненасыщенные и пересыщенные
- Влияние растворимости на свойства растворов
- РАСТВОРЕНИЕ КАК ФИЗИКО-ХИМИЧЕСКИЙ ПРОЦЕСС
- Видео:
- Растворение. Растворимость веществ в воде | Химия 8 класс #39 | Инфоурок
Как называется процесс взаимодействия растворимого вещества с водой?
Растворение — это физико-химический процесс, при котором растворяемое вещество, называемое сольватом или растворяемым компонентом, взаимодействует с растворителем, в данном случае — с водой. В результате этого взаимодействия происходит образование раствора, состоящего из растворителя и растворенного компонента.
Водные растворы являются наиболее распространенными примерами растворов и впервые были изучены учеными Менделеевым и Менчиковым. В процессе растворения молекулы растворимого вещества, или растворенного компонента, вступают во взаимодействие с молекулами растворителя, образуя группы межмолекулярных связей, называемые сольватацией. Данное взаимодействие происходит одновременно с поглощением и выделением теплоты.
Растворимость — это представление о количестве растворимого компонента, которое может раствориться в данном растворителе при определенных условиях. Растворимость может быть постоянной или переменной и зависит от физико-химических свойств растворимого вещества и растворителя, а также от условий температуры и давления.
Понятие о растворах Растворимость веществ
Одним из основных понятий, описывающих процесс растворения, является растворимость. Растворимость – это мера способности вещества раствориться в определенном количестве растворителя при определенной температуре.
Растворимость зависит от химического состава вещества и физических условий растворения, таких как температура и давление. В результате растворения образуются растворы разных состояний – газообразные, жидкие и твердые. Газообразные растворы представлены газами в жидкости или паре над ней. Жидкие растворы могут быть представлены однородной жидкостью, или жидкостью в жидкости. Твердые растворы представляют собой гомогенную систему, состоящую из твердого растворителя и одного или нескольких растворенных компонентов, которые могут быть растворены в твердом растворителе.
Сольватация и гидратация
В процессе растворения вода взаимодействует с растворенным веществом с помощью солватации и гидратации. Солватация – это процесс образования гомогенной системы, состоящей из молекул растворителя и растворенного вещества. Гидратация – это процесс образования гомогенной системы, в которой молекулы растворителя окружают растворенные и образуют гидраты. Гидраты являются растворимыми веществами, в которых растворители находятся в виде замороженного гидрата.
Растворы насыщенные, ненасыщенные и пересыщенные
Раствор называется насыщенным, если при данной температуре и давлении в нем содержится максимальное количество растворенного вещества, которое может быть растворено в этом растворителе. Ненасыщенным раствором называется раствор, в котором содержится меньшее количество растворенного вещества, чем максимальное. Пересыщенные растворы содержат большее количество растворенного вещества, чем максимальное, и в результате могут произойти процессы кристаллизационной поглощения.
Влияние растворимости на свойства растворов
Растворимость веществ зависит от химического состава вещества, температуры, давления и других факторов. Ученые, в частности, Дмитрий Иванович Менделеев, изучали растворимость различных веществ и разделили их на группы в зависимости от их растворимости в воде. Некоторые вещества хорошо растворяются в воде, образуя растворы разных цветов, такие как сульфаты, которые являются сильными электролитами. Другие вещества практически нерастворимы в воде, например, некоторые соединения газов.
РАСТВОРЕНИЕ КАК ФИЗИКО-ХИМИЧЕСКИЙ ПРОЦЕСС
Растворение может происходить одновременно со снятием и добавлением растворённого вещества. Растворённое вещество, которое растворяется в воде или другом растворителе, называется растворителем, а процесс, при котором это происходит, называется растворением. Растворители и растворённые вещества могут быть разных типов, таких как полярные и неполярные соединения.
Растворимость растворимого вещества зависит от различных факторов, таких как температура, свет, счетное соотношение между растворителем и растворённым веществом, наличие других компонентов в растворе и т. д. Например, растворимость сульфата в воде зависит от температуры: чем больше температура, тем больше растворимость сульфата.
Растворённое вещество может быть в форме кристаллов, которые образуются при кристаллизационной гидратации или сольватации. Кристаллы представляют собой молекулы растворимого вещества, которые поглощают молекулы растворителя и образуют постоянную структуру в растворе. Кристаллы обладают определенной формой и могут быть видимыми в свете или меньше, чем раковина.
- Растворение зависит от температуры, при которой растворение происходит. Наибольшую растворимость достигают в горячих растворах, а наименьшую в холодных.
- Растворимость растворимого вещества воде зависит от энергии решетки. Растворимость увеличивается с увеличением энергии решетки и уменьшается с увеличением полярности раствора.
- Растворимость может быть переменной в разных растворителях. Например, йод имеет большую растворимость в этаноле, но меньшую в воде.
- Гидратация — это процесс образования гидратов, при котором молекулы растворителя проникают внутрь молекулы растворённого вещества.
- Сольватация — это процесс образования сольватных комплексов, при котором молекулы растворителя окружают молекулы растворённого вещества.
Таким образом, растворение представляет собой сложный физико-химический процесс, в котором происходит взаимодействие между различными компонентами — растворителем и растворённым веществом. Растворение важно для понимания химических реакций и многих других явлений, связанных с взаимодействием веществ в растворах.
Видео:
Растворение. Растворимость веществ в воде | Химия 8 класс #39 | Инфоурок
Растворение. Растворимость веществ в воде | Химия 8 класс #39 | Инфоурок by ИНФОУРОК 69,367 views 6 years ago 9 minutes, 19 seconds