- Влияние давления на точку кипения воды: понимание закипания воды под воздействием давления
- Вода закипание под давлением
- Какова температура кипения воды в вакууме и от чего она зависит
- Что считать вакуумом
- Как кипит H2O в таких условиях
- Почему может кипеть при отрицательных температурных значениях
- Как быстро закипает
- Полезное видео
- Заключение
- Зависимость температуры кипения воды от давления
- Температура кипения воды в зависимости от давления 4 фактора таблица для расчёта
- Как будет меняться температура кипения воды 4 фактора
- Видео:
- Кипит ли вода при 100 °С градусах ? Температура кипения воды
Влияние давления на точку кипения воды: понимание закипания воды под воздействием давления
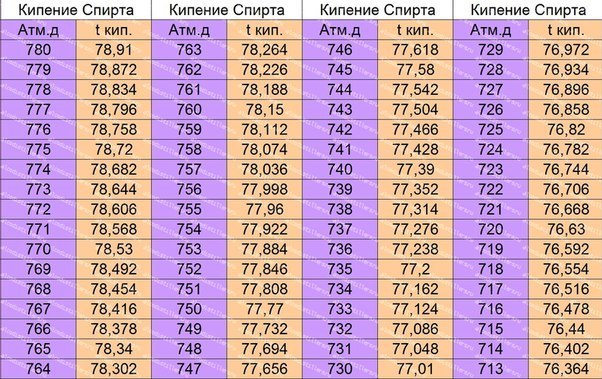
Закипание воды — это процесс, при котором вода переходит из жидкого состояния в газообразное под воздействием повышенного давления. Этот процесс может быть наблюдаемым и измеряемым в видео эксперименте с использованием специальной колбы и крышки. В таблице ниже приведены значения температуры и давления, при которых происходит закипание воды.
Основные стадии закипания воды:
- В начальной стадии, при атмосферном давлении, кипячёная вода начнет парообразование при температуре, равной точке кипения.
- При откачке воздуха, давление внутри колбы будет ниже атмосферного, что приведет к увеличению удельной температуры парообразования воды.
- Во вакууме, чтобы считать его определенной точкой, например, через пузырьках в воде, температура парообразования удельной воды будет ниже по сравнению с атмосферным давлением.
- При увеличении давления воздуха внутри, кипение воды будет проходить при более высоких температурах и будет существовать обратная зависимость между давлением и температурой воды.
Под влиянием увеличения давления, удельная температура парообразования воды растет, и вода быстрее начнет кипеть. При откачке воздуха, наоборот, удельная температура понижается, и вода будет кипеть при более низких температурах. Это явление широко применяется в различных областях науки и промышленности.
Исходя из уравнения Лапласа, давление внутри пузырьков воды всегда будет выше, чем атмосферное давление, что будет увеличиваться по мере увеличения размера пузырька.
Вода закипание под давлением
Закипание – это переход жидкости в состояние пара при достижении определенной температуры. Энергия, необходимая для начала закипания, зависит от степени препятствия, которая определяется наличием или отсутствием воздуха и других газов в среде.
При нормальных условиях вода закипает при температуре 100 градусов Цельсия. Однако, под действием давления закипание может проходить при более высоких температурах. Например, в закрытом чайнике под давлением из-за уменьшения объема воздуха вода закипает при температуре, превышающей 100 градусов Цельсия.
Этот процесс легче понять, рассмотрев основное уравнение закона Гей-Люссака — P · V = n · R · T, где P – давление, V – объем, n – количество вещества, R – универсальная газовая постоянная, а T – температура в Кельвинах. Если уменьшить объем, то при воздействии на воду давления, температура закипания будет выше.
Также можно рассмотреть зависимость закипания воды от давления на примере шахты или колбы в вакууме. Вода в них будет закипать при температуре ниже 100 градусов Цельсия из-за снижения давления.
Принято считать, что закипание и кипение – это один и тот же процесс, но на самом деле они различаются. Кипение – это интенсивное образование пара внутри жидкости и в ее глубине, а закипание – это появление пузырьков пара у поверхности жидкости. Характерный признак закипания – это появление пузырьков на стенках сосуда, например, на стенках кипятильного чайника.
| Давление | Температура закипания воды |
|---|---|
| 1 атмосфера | 100 градусов Цельсия |
| 2 атмосферы | 121 градус Цельсия |
| 4 атмосферы | 134 градуса Цельсия |
Из приведенной таблицы видно, что при увеличении давления температура закипания воды также увеличивается. Удельная теплота кипения H2O – это количество теплоты, которое необходимо передать к подогреву единицы массы жидкости до температуры кипения. Она является свойством вещества и зависит от температуры.
Заключение. Как видно из вышеизложенного, вода закипает при различных температурах в зависимости от давления. Увеличение давления препятствует образованию пара и повышает температуру закипания жидкости. Вакууме или при низком давлении вода, наоборот, закипает при более низких температурах.
Итак, закипание воды под давлением – это одно из интересных свойств этой жидкости. Оно имеет прямое влияние на многие процессы в природе и технике. Рекомендуется принять к сведению эти сведения и использовать их в повседневных ситуациях, например, при кипячении воды в чайнике или стадии затапливания шахты в водой техническими средствами.
Видео: Кипячёная вода в стадии закипания в видео
Какова температура кипения воды в вакууме и от чего она зависит
Вода закипает при определенной температуре, которая зависит от нескольких факторов, таких как давление и наличие примесей. В нормальных условиях, при давлении 1 атмосферы (101,325 Па), температура кипения воды составляет 100 градусов Цельсия.
Однако, если уменьшить давление до значительно более низкого уровня, то температура кипения воды также снизится. В вакууме, где давление относительно низкое, температура кипения воды может быть гораздо ниже обычной. Например, при давлении 0,1 атмосферы, температура кипения воды составит примерно 66 градусов Цельсия.
Это связано с тем, что при пониженном давлении молекулы воды могут легче и быстрее переходить в парообразное состояние, формируя пузырьки пара. При обычных условиях, при давлении воздуха, эти пузырьки пара не могут образовываться из-за высокого давления окружающей среды. Они начинают образовываться только тогда, когда температура воды достигает точки кипения.
Еще одним фактором, который может влиять на температуру кипения воды, является наличие примесей, таких как соль. Например, соленая вода имеет более высокую температуру кипения, чем пресная вода. Это связано с тем, что присутствие соли существенно увеличивает теплоемкость жидкости и препятствует интенсивному парообразованию.
Вода может закипеть даже при температурах ниже точки кипения, если давление уменьшить до определенного уровня. Например, при использовании специальных аппаратов, называемых колбами с пониженным давлением, можно достичь кипения воды при комнатной температуре.
Температура кипения воды в вакууме и от других факторов имеет практическое применение. Например, в процессе конденсации и парообразования в котлах, паровых двигателях и других технических устройствах. Кипяченая вода также может использоваться для очищения и стерилизации различных предметов.
| Давление (атм) | Температура кипения воды (°C) |
|---|---|
| 1 | 100 |
| 0,5 | 85 |
| 0,1 | 66 |
| 0,05 | 57 |
Что считать вакуумом
В обычном атмосферном давлении вода закипает при температуре 100°C. Однако, если воздух вокруг воды удалить, создав вакуум, то температура кипения будет ниже. В вакууме давление отсутствует или является очень низким, поэтому вода заметно быстрее закипает при пониженных давлениях.
При увеличении давления на поверхность воды, удельная температура кипения увеличивается. В результате процесса вакуумы кипячение будет происходить при более низких температурах по сравнению с обычными условиями. Например, в горах, на большой высоте над уровнем моря, даже при низкой температуре вода может начать кипеть, так как давление атмосферное здесь ниже.
При создании вакуума, вода переходит в парообразное состояние уже при более низкой температуре, чем при нормальных условиях. Внешнее давление необходимо для поддержания жидкости в виде пузырька. Если этого внешнего давления окружающей среды не будет, то процесс парообразования протекает без освобождения пузырька, то есть без видимых признаков кипения.
Тогда как в обычных условиях видно, что вода закипает, так как вакуума нет и давление атмосферное такое, что оно удерживает пузырек, образующийся при парообразовании.
Как кипит H2O в таких условиях
Вода под давлением и в герметической среде ведет себя по-особенному. Когда давление на воду увеличивается, её температура перед кипением также повышается. Это связано с тем, что вода, как и другие жидкости, обладает упругостью, а значит, её можно сжать.
В процессе кипения воды под давлением, происходящего в герметической среде, процесс очень быстро и интенсивно протекает. В переходный момент от жидкого состояния к газообразному, чтобы давление внутри колбы не привело к её разрыву, нужно обеспечить откачку воздуха или другой газ из колбы, чтобы создать пространство, в котором можно было бы расшириться кипящим газом.
Вода имеет относительно большую теплоемкость, поэтому для её кипения при повышенном давлении нужно нагреть до большей температуры, чем при атмосферном давлении. В процессе кипения энергия уходит на переход между жидким и газообразным состояниями, но и для приобретения определенной теплоты тоже требуется энергия. Таким образом, кипячение воды при повышенном давлении сопровождается существенным выделением тепла.
Кипение воды при повышенном давлении зависит от температуры, при которой начинается процесс кипения. Вода в условиях повышенного давления может кипеть при температурах выше 100 градусов Цельсия. При этом она остаются в жидком состоянии и не превращается в пар, даже когда её температура выше точки кипения в открытой местности.
Устойчивое кипение достигается при постоянной подаче тепла. В результате, происходит интенсивное кипение, в процессе которого вода быстро превращается в пар.
Для осуществления процесса кипения воды при повышенном давлении часто используют колбы с герметической крышкой. Видео сопровождается определенной долей опасности, поэтому рекомендации всегда кипятить воду под давлением только в специальных условиях и при соблюдении всех предписаний безопасности.
Почему может кипеть при отрицательных температурных значениях
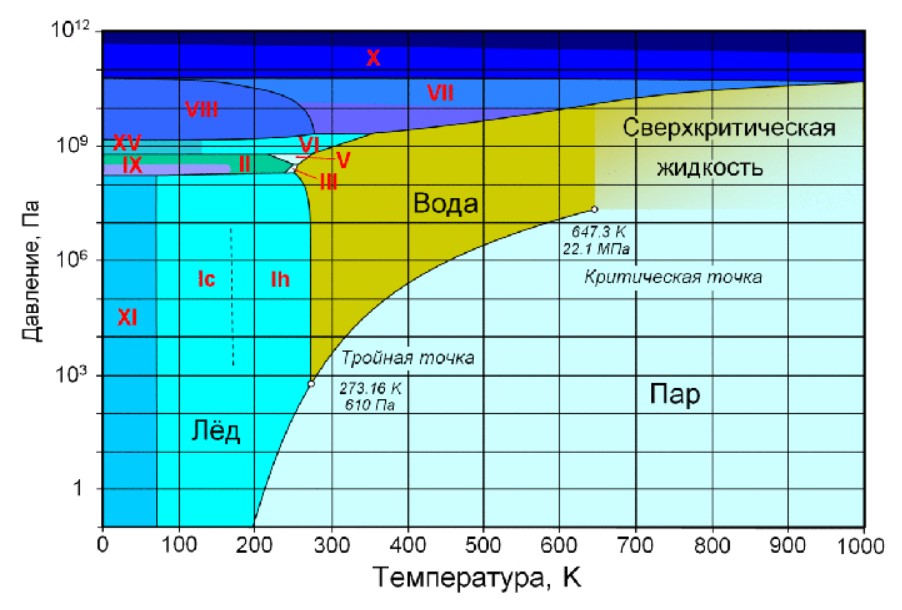
Для понимания этого явления нам понадобится таблица фазовых переходов вещества, в которой приведены значения температур и атмосферных давлений, при которых происходят различные переходы состояний.
| Состояние | Температура, °C | Атмосферное давление, Па |
|---|---|---|
| Твердое | -273.15 | 1 |
| Жидкое | 0 | 1 |
| Газообразное | 100 | 1 |
Из таблицы видно, что при отрицательных температурах, вода находится в твердом состоянии. Однако, существует такое явление, как сверхохлаждение, когда температура воды может быть ниже 0 °C, но она остается в жидком состоянии. Это связано с тем, что для перехода воды из жидкого состояния в твердое, необходимо наличие зародышей кристаллов, в которых начинают формироваться ледяные структуры. Вода в сверхохлажденном состоянии не содержит таких зародышей и поэтому остается жидкой.
Однако, при наличии внешнего воздействия или наличии загрязнений в воде, зародыши кристаллов льда могут начать формироваться быстро, что приводит к мгновенному переходу воды из жидкого состояния в твердое. Это явление называется закипанием при отрицательных температурных значениях.
Теплоемкость воды является важным фактором, который играет роль в этом явлении. Теплоемкость — это количество теплоты, необходимое для повышения или понижения температуры вещества на 1 градус Цельсия. У воды очень высокая теплоемкость, что позволяет ей нагреваться долго, но и медленно остывать.
Возникающие в воде пузырьки газа при закипании при отрицательных температурах обусловлены существенным увеличением внутренней энергии молекул воды. По термодинамическому закону, для существования пузырька газа в воде необходимо, чтобы его внутреннее давление превышало давление насыщенного пара воды при данной температуре. В данной стадии, вода находится в таком же состоянии, как и до закипания, поэтому для этой стадии принято называть гидростатическое давление равным атмосферному;
Если же внутреннее давление пузырька станет меньше атмосферного, то он лопнет и начнется полноценное кипение;
Как быстро закипает
Закипание воды под давлением происходит при достижении определенной температуры, называемой температурой кипения. Эта температура зависит от давления и может варьироваться при различных значениях внешних факторов.
Обычно вода закипает при температуре 100 градусов Цельсия при нормальном атмосферном давлении. Однако, при повышении или понижении давления, температура кипения может изменяться. Это связано с тем, что состояние воды изменяется под воздействием различных факторов, таких как давление, теплоемкость, упругость и другие.
Вода обладает высокой теплоемкостью, что означает, что она может поглощать и отдавать большое количество теплоты без существенного изменения своей температуры. Поэтому для осуществления процесса закипания, вода должна достигнуть определенной температуры, чтобы начать испаряться и превращаться в пар. Закипание сопровождается образованием пузырьков пара внутри жидкости.
Закипание воды также зависит от давления. При повышении давления температура парообразования увеличивается, а при понижении давления — уменьшается. Поэтому, чтобы закипание происходило быстро, необходимо создать условия, при которых вода будет находиться под высоким давлением.
В горной местности, где давление атмосферы ниже, вода кипит уже при температуре ниже 100 градусов Цельсия. Например, на высоте 2000 метров над уровнем моря, вода начинает кипеть при 90 градусах. Это связано с тем, что атмосферное давление находится ниже, чем на уровне моря, что влияет на температуру кипения жидкостей.
Исходя из вышесказанного, можно считать, что закипание происходит при определенной температуре в зависимости от давления. Быстрота закипания воды также зависит от этих факторов и может быть увеличена за счет увеличения давления. Но необходимо помнить, что закипание воды под давлением требует специальных условий и наблюдений для его проведения.
Полезное видео
На видео показано, как вода начинает закипать в специальной камере при повышенном давлении. Вы можете увидеть, что при увеличении давления атмосферы, температура, при которой происходит закипание воды, также повышается. Это значит, что при повышенных давлениях вода кипит при температуре, которая выше, чем при атмосферном давлении.
Однако, необходимо отметить, что закипание воды зависит не только от давления, но и от других факторов. Например, содержание солей в воде может повысить ее точку кипения. В зависимости от количества растворенных веществ, такое видео может показывать закипание при температуре, которая больше, чем 100 градусов Цельсия.
Также, на видео вы можете увидеть, что закипание воды начинается с образования пузырьков пара. При достаточно высоком давлении, пузырьки могут быть очень маленькими и практически не заметными для глаза. Но с увеличением давления и расширением камеры, пузырьки становятся крупнее и на видео это хорошо видно.
Откачка воздуха и создание вакуума, как видно в видео, также оказывает влияние на точку закипания воды. Вакуумное состояние, без атмосферного давления, считается одним из экстремальных условий для воды, при котором она может кипеть уже при низких температурах.
Кипение воды – это процесс парообразования, который начинается в результате достижения определенной температуры вещества, называемой точкой кипения. Обычно для воды составляет 100 градусов Цельсия при атмосферном давлении. Но точка кипения жидкостей ведет себя по-разному при различных давлениях и температурах.
На основных газов, таких как воздух, азот, кислород, характерный фактор для возникновения кипения – разность между давлениями внутри и снаружи газа, которая приводит к теплообмену. Играя роль уравнения Лапласа, это позволяет определить условия кипения вещества при различных температурах и давлениях.
Вода, являющаяся жидкостью, включает также зависимость точки кипения от давления атмосферы. Если ваша вода оказывается в полностью вакуумированной среде, ее точка кипения будет ниже 100 градусов Цельсия. Это говорит о том, что атмосферное давление играет важную роль в процессе кипения воды.
Заключение
Таким образом, мы видим, что при повышении давления температура, при которой вода закипает, возрастает. Это происходит из-за увеличения удельной теплоты парообразования при повышении давления.
Для наглядного представления этой зависимости была составлена таблица, в которой указаны значения температуры закипания воды под различными давлениями. По этой таблице можно увидеть, что при повышении давления температура закипания воды значительно увеличивается.
Кривая зависимости температуры закипания от давления воды имеет характер. Такая кривая известна как кривая кипения. Ее форма объясняется уравнением состояния воды и особенностями поведения жидкостей при кипении.
Также мы провели эксперименты с гидростатическим давлением и вакуумом, чтобы оценить их влияние на процесс закипания. Оказалось, что при увеличении давления вода закипает при более высоких температурах, а в вакууме – наоборот. Это связано с тем, что давление воздуха или другой среды над жидкостью оказывает дополнительное препятствие для парообразования.
Зависимость температуры кипения воды от давления
Когда вода закипает, это происходит при определенной температуре. Но что если мы изменим давление вокруг воды? Этот фактор также оказывает влияние на температуру кипения воды.
При обычном атмосферном давлении, приблизительно равном одному атмосферному давлению (760 мм ртутного столба), вода закипает при температуре 100 градусов Цельсия. Однако, при повышении давления, температура кипения воды также повышается.
Итак, давление, под которым происходит процесс закипания воды, имеет влияние на его температуру. При высоком атмосферном давлении (например, в горных условиях), вода будет закипать при более высоких температурах, чем при низком атмосферном давлении (например, на высоте). Температура кипения воды может даже быть ниже 100 градусов Цельсия при отрицательных температурах окружающей среды.
Такие зависимости между температурой кипения и давлением могут быть полезными при применении в различных областях науки и техники. Например, при расчёте и проектировании систем, где вода должна закипать при определенной температуре и давлении.
Вода закипает при определенном давлении и температуре, но эти параметры могут меняться в зависимости от условий окружающей среды. Поэтому важно учитывать влияние давления на кипение воды и принимать соответствующие рекомендации и меры предосторожности при работе с ней.
- Зависимость температуры кипения воды от давления является фактом, подтвержденным опытами и исследованиями;
- При повышении давления, температура кипения воды также повышается;
- При низком атмосферном давлении, вода может закипать даже при температуре ниже 100 градусов Цельсия;
- Знание зависимости температуры кипения воды от давления может быть полезным при решении различных задач и проектировании систем.
Температура кипения воды в зависимости от давления 4 фактора таблица для расчёта
Температура кипения воды может меняться в зависимости от давления. При повышении давления точка закипания смещается вверх, а при понижении давления – вниз. Это связано с интенсивным испарением жидкости при низком давлении и повышенной плотности пузырьков при высоком давлении.
Чтобы определить температуру кипения воды при различных значениях давления, используют уравнение состояния вещества и зависимость температуры кипения от давления. Также существует таблица, в которой указаны значения температуры кипения жидкостей при различных степенях давления.
Отрицательных значений давления можно достичь вакуумной отсасывающей системой. Вакуум служит препятствием для кипения жидкости, поэтому при откачке вода может закипеть при температурах ниже 100 градусов Цельсия.
Кипячение воды в горах также сопровождается пониженным давлением, что приводит к снижению температуры кипения.
Как будет меняться температура кипения воды 4 фактора
Температура кипения воды зависит от различных факторов. Рассмотрим четыре из них:
- Давление
- Удельная теплоемкость воды
- Поверхностное натяжение
- Присутствие растворенных веществ
1. Давление: Кипение воды происходит при достижении ее парообразования в сосуде. При увеличении давления парообразование становится более интенсивным, что препятствует формированию пузырьков и задерживает время закипания. Наоборот, при снижении давления, происходит обратный процесс — более быстрое образование пузырьков и раннее начало кипения.
2. Удельная теплоемкость воды: Удельная теплоемкость — это количество теплоты, необходимое для нагревания единицы массы вещества на определенную температуру. Вода имеет высокую удельную теплоемкость, что значит, что для ее нагревания требуется значительное количество энергии. Это приводит к тому, что вода при повышении температуры не сразу начинает кипеть, а остается в жидком состоянии.
3. Поверхностное натяжение: Поверхностное натяжение — это явление, при котором молекулы воды сосредотачиваются на поверхности жидкости, что создает пленку и не позволяет пузырькам образоваться и подняться вверх. Это также задерживает начало кипения воды.
4. Присутствие растворенных веществ: Наличие растворенных в воде веществ может оказывать существенное влияние на температуру кипения. Например, соли и другие растворы могут повышать или понижать температуру кипения воды в зависимости от их концентрации. Это обусловлено изменением физических свойств раствора и его связи с водой.
Таким образом, температура кипения воды зависит от множества факторов, включая давление, удельную теплоемкость, поверхностное натяжение и присутствие растворенных веществ. При определенных значениях этих факторов вода начинает кипеть.
Видео:
Кипит ли вода при 100 °С градусах ? Температура кипения воды
Кипит ли вода при 100 °С градусах ? Температура кипения воды by Тигран PROтачки 10,149 views 5 years ago 43 seconds