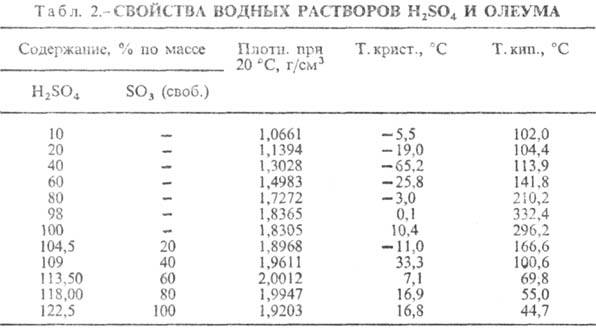
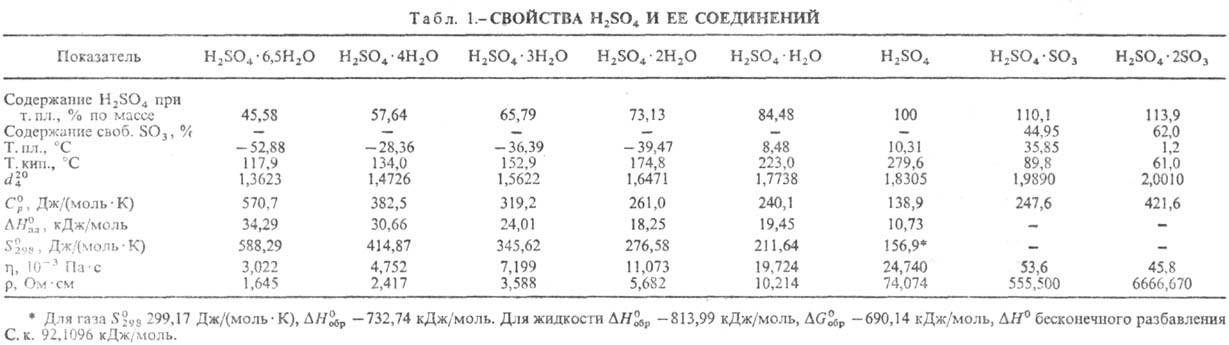
Измерение концентрации серной кислоты в воде
Химия – наука о строении, свойствах и превращениях веществ. В химии существует множество задач, связанных с решением различных расчетов. Одной из таких задач является вычисление концентрации серной кислоты в воде.
Серная кислота (H2SO4) – одна из самых распространенных химических веществ, используемая в различных отраслях промышленности. Она может быть растворена в воде, образуя раствор с определенной концентрацией. Для решения данной задачи необходимо использовать закон Рауля и умение проводить расчеты по формулам химических реакций.
Задача на вычисление концентрации серной кислоты в воде может быть решена следующим образом. Сначала необходимо определить количество растворенного в воде железа. Затем, используя молярную массу серной кислоты и массу железа, вычислить концентрацию серной кислоты в растворе.
Концентрация серной кислоты может быть выражена в различных единицах измерения, таких как молярность, нормальность и процентная концентрация. В данной задаче мы будем использовать массовую концентрацию, выраженную в граммах серной кислоты на литр воды.
ХимикПРО – решение задач по химии бесплатно
На сайте ХимикПРО вы можете бесплатно решить задачи по химии, связанные с определением концентрации различных растворов. В химии концентрация растворов играет важную роль, поскольку она позволяет определить количество вещества, растворенного в данном растворителе.
Одним из методов определения концентрации является рассчет количества вещества в растворе с использованием нормальной молярной массы. Например, для определения концентрации серной кислоты в воде можно взять определенный участок этой кислоты, растворить его в определенном объеме воды и рассчитать массовую долю серной кислоты.
Когда мы знаем массу растворителя, объем паров необходимый для растворения данного количества кристаллов, мы можем оприходовать на растворение данного количества железа. Если мы знаем растворимость вещества на одного литра данного раствора, то по мольной концентрации можем представить раствор в виде данного уравнения:
M/n=nравно*V-2/(V=10)
где:
M — молярная масса железа;
n — количество молей железа;
nравно — количество эквивалентов железа;
V-2 — объем паров железа, участвующих в реакции;
V=10 — объем раствора бария.
Таким образом, растворенная часть железа в данном растворе будет определяться массой железа, необходимой для реакции с барием. Из этого уравнения мы можем рассчитать концентрацию серной кислоты в воде.
Напомню, что концентрация раствора — это отношение массы вещества к объему раствора. В данной задаче мы рассчитываем концентрацию серной кислоты в воде по количеству эквивалентов железа, реагирующих с барием.
На сайте ХимикПРО вы найдете решение подобных задач по химии, возможно, вы уже не раз сталкивались с ними в своей учебе. Конечно, задачи по химии могут быть сложными, но с помощью ХимикПРО вы сможете успешно разобраться в них и решить поставленные задачи.
Ответ
Для решения данной задачи по определению концентрации серной кислоты в водном растворе необходимо использовать формулу, которая выражается через массу кислоты и объем растворителя. Данная задача относится к участку задач, связанных с расчетами концентраций растворов и расчетов по объемам
Для решения данной задачи можно использовать разные подходы. Один из самых простых и широко используемых подходов — это использование закона Рауля. Согласно данному закону, концентрация растворенного вещества в паре избыточного раствора пропорциональна молярной доле этого вещества в растворителе.
Для вычисления концентрации серной кислоты в водном растворе можно использовать молярность и нормальность данной кислоты. Молярность — это количество молей кислоты в 1 литре раствора, а нормальность — число грамм-эквивалентов кислоты в 1 литре раствора.
Для расчетов обычно используют массу кислоты, молярность, нормальность и моляльность.
Для расчета концентрации серной кислоты в воде по ее массе и объему раствора можно воспользоваться следующей формулой:
- Пересчитаем массу кислоты в атомных единицах (моль), используя молярную массу серной кислоты.
- Рассчитаем количество молей серной кислоты в полученном растворе, используя массу и молярность.
- Рассчитаем количество грамм-эквивалентов серной кислоты в полученном растворе, используя массу и нормальность.
- Рассчитаем моляльность серной кислоты в водном растворе, используя массу и объем раствора.
- Расчеты по расчетам концентрации растворов серной кислоте в объемном выражении.
Таким образом, чтобы вычислить концентрацию серной кислоты в водном растворе, необходимо знать массу кислоты, молярность и нормальность кислоты, а также объем раствора. Используя вышеописанные формулы и расчеты, можно рассчитать концентрацию серной кислоты и получить ответ на данную задачу.
Задачи с решениями на концентрацию растворов
Химическая концентрация может быть выражена в различных единицах, таких как молярность, моляльность, нормальность и массовая доля. В данном разделе мы рассмотрим задачи на расчет концентрации растворов по молярной и массовой концентрации.
Приведем первую задачу. Если 100 г некоторого раствора серной кислоты содержат 2 моль этого вещества, то какая молярность этого раствора?
Решение: согласно закону Рауля, вся составляющая вещества имеет одну и ту же концентрацию и найдем ее. Количество вещества в растворе определяем по формуле:
Молярность = количество вещества / объем раствора
Тогда, в данной задаче, нам известно, что 100 г раствора содержат 2 моля серной кислоты, поэтому можно рассчитать концентрацию:
Молярность = 2 моль / 100 г = 0,02 моль/г
Таким образом, концентрация раствора серной кислоты составляет 0,02 моль/г.
Другая задача связана с определением массы растворителя, необходимой для растворения заданной массы вещества. Например, сколько граммов воды нужно использовать для растворения 500 г кристаллов глюкозы?
Решение: для рассчета массы растворителя в данной задаче мы должны знать концентрацию раствора глюкозы. Так как глюкоза является молекулой неэлектролита, то концентрация раствора глюкозы будет равна массовой доле вещества в растворе:
Массовая концентрация = масса вещества / масса растворителя
Тогда, в данной задаче, если мы знаем массу глюкозы в растворе (500 г), то можем рассчитать массу воды:
Масса растворителя = масса глюкозы / массовая концентрация = 500 г / 1 = 500 г
Таким образом, для растворения 500 г кристаллов глюкозы необходимо использовать 500 г воды.
В этом разделе мы рассмотрели лишь две задачи на расчет концентрации растворов, однако в химии существует множество других задач, связанных с определением концентрации. Знание основных методов и формул позволяет успешно решать такие задачи и получать необходимые результаты в химических экспериментах.
Концентрация растворов Растворы неэлектролитов Растворимость
Количество растворимого вещества можно измерить по массе, молекулярной массе и числу молекул вещества. Количество вещества можно выразить в молях, массах или объемах. При разбавлении раствора его концентрация уменьшается, так как количество вещества остается неизменным, а объем раствора увеличивается.
В растворах неэлектролитов существуют различные способы выражения концентрации. Одним из таких способов является мольная концентрация (моляльность). Моляльность показывает количество молей растворенного вещества в одном килограмме растворителя. Масса растворенного вещества можно найти с помощью формулы: масса = масса раствора – масса воды. Формула моляльной концентрации имеет вид: моляльность = количество вещества / масса растворителя.
В задачах по растворам, часто встречаются задачи на решение расчетов массы вещества, растворенного в определенном объеме раствора или на расчет массы вещества, осаждается или образуется при реакции растворов.
Расчеты концентрации растворов неэлектролитов и растворов электролитов могут быть разными, так как молекулярная масса растворимого вещества, его диссоциация и число молекул вещества в растворе могут отличаться. Однако, сама концентрация раствора в обоих случаях рассчитывается по аналогичным принципам.
Для определения концентрации вещества в растворе можно использовать различные методы, такие как определение массы вещества, концентрация раствора по массе, определение объема раствора, анализ парами и т.д. Решение задач по концентрации растворов вода и других веществ бесплатно доступно на специальных сайтах.
Видео:
Льем воду в кислоту. Шок контент. Химия – Просто
Льем воду в кислоту. Шок контент. Химия – Просто автор: Химия – Просто 801 288 переглядів 6 років тому 7 хвилин і 1 секунда